题目内容
【题目】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的结构简式为____________,A的官能团为_________(填名称)。
(2)下列物质中,不能通过乙烯加成反应得到的是_________(填序号)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(3)已知2CH3CHO+O2 ![]() 2CH3COOH若以乙烯为主要原料合成乙酸,其合成路线如下图所示:
2CH3COOH若以乙烯为主要原料合成乙酸,其合成路线如下图所示:![]()
a. 反应②的化学方程式为______________________________。
b. 工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为______________________________,反应类型是______________。
【答案】 CH2=CH2 羟基 B 2CH3CH2OH+O2![]() 2CH3CHO+2H2O nCH2=CH2
2CH3CHO+2H2O nCH2=CH2![]()
![]() 加聚反应
加聚反应
【解析】试题分析:(1)乙烯分子中含有碳碳双键,结构简式为CH2=CH2;乙烯与水发生加成反应,生成乙醇,乙醇被氧化为乙醛,乙醛被氧化为乙酸。所以A是乙醇,官能团的名词为羟基;
(2)A、乙烯与氢气发生加成反应生成乙烷,正确;B、乙烯与HCl加成或与氯气加成都无法得到CH3CHCl2,错误;C、乙烯与水发生加成反应生成乙醇,正确;D、乙烯与HBr发生加成反应生成溴乙烷,正确,答案选B。
(3)a、反应②为乙醇的催化氧化反应,生成乙醛和水,化学方程式是2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
b、乙烯发生加聚反应,生成聚乙烯,化学方程式是nCH2=CH2![]()
![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
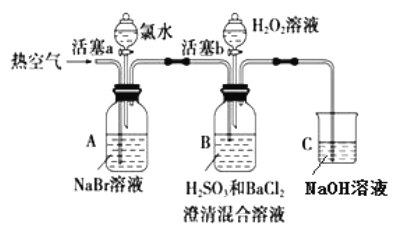
小学生10分钟应用题系列答案【题目】某小组同学为探究 H2O2、 H2SO3、 Br2 氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
实验记录如下:
实验操作 | 实验现象 | |
① | 打开活塞 a,滴加氯水,关闭活塞 a | _____________________________________________ |
② | 吹入热空气一段时间后停止 | A中溶液颜色明显变浅;B中有气泡,产生大量白色沉淀,沉降后上层清液为无色 |
③ | 打开活塞b,逐滴加入H2O2溶液 | 开始时溶液颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成橙红色。 |
完成下列填空:
(1)在进行操作①时,A中的实验现象是___________,有关反应的离子方程式是___________。
(2)操作②吹入热空气的目的是____________。B 中产生白色沉淀的化学式是___________。
(3)装置C的作用是____________________。
(4)由上述实验可知,在此实验条件下,H2O2、H2SO3、Br2氧化性强弱顺序为________________。
(5)操作③开始时颜色无明显变化可能原因是(写出一条即可):___________________。
【题目】下图是利用废铜屑(含杂质)制备胆矾(硫酸铜晶体)的过程
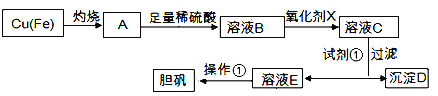
已知:
溶液中被沉淀的离子 | Fe3+ | Fe2+ | Cu2+ |
完全生成氢氧化物的沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
请回答:
(1)下列物质中最适宜做氧化剂X的是________(填字母)。
A. NaClO B. H2O2 C.KMnO4
(2)加入试剂①是为了调节pH,试剂①可以选择________(填化学式)。
(3)操作①的名称是________。
(4)沉淀D加入盐酸可以得到FeCl3溶液,关于FeCl3溶液的性质中说法不正确的是________。
A. 将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
B. 向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
C. 将FeCl3溶液滴加NaOH溶液,将沉淀干燥灼烧,得到Fe(OH)3固体
D. 向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(5) 沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉防止FeCl2溶液变质,其原因是________________(用离子方程式表示)。