题目内容
【题目】由某精矿石(MCO3·ZCO3)可以制备单质M,制备过程中排放出的二氧化碳可以作为原料制备甲醇,取该矿石样品1.84g,高温灼烧至恒重,得到0.96g仅含两种金属氧化物的固体,其中m(M)︰m(Z)=3:5,请回答:
(1)该矿石的化学式为______________。
(2)①以该矿石灼烧后的固体产物为原料,真空高温条件下用单质硅还原,仅得到单质M和一种含氧酸盐(只含Z、Si和O元素,且Z和Si的物质的量之比为2︰1)。写出该反应的化学方程式____________________________________________。
②单质M还可以通过电解熔融MCl2得到,不能用电解MCl2溶液的方法制备M的理由是_______________________________________________________________。
(3)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1:CO2(g)+H2(g)CO(g)+H2O(g) △H1
反应2:CO(g)+2H2(g)CH3OH(g) △H2
反应3:CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H1
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图1所示。
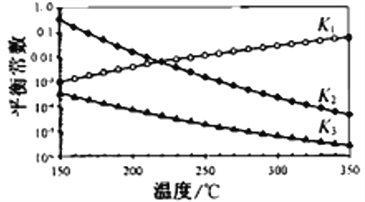
则△H1_______△H2 (填“大于”、“小于”、“等于”),理由是______________________。
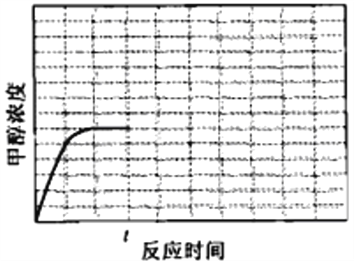
(4)在温度T1时,使体积比为3︰1的H2和CO2在体积恒定的密闭容器内进行反应。T1温度下甲醇浓度随时间变化曲线如图2所示;不改变其他条件,假定t时刻迅速降温到T2,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线。
【答案】 MgCO3CaCO3 2MgO+2CaO+Si![]() 2Mg+Ca2SiO4 电解MgCl2溶液时,阴极上H+比Mg2+容易得到电子,电极反应式为2H2O+2e-=H2↑+2OH-,所以得不到镁单质 小于;曲图l可知,随着温度升高,K1增大,则△H1>0,根据盖斯定律又得△H3=△H1+△H2,所以△H2<△H3;
2Mg+Ca2SiO4 电解MgCl2溶液时,阴极上H+比Mg2+容易得到电子,电极反应式为2H2O+2e-=H2↑+2OH-,所以得不到镁单质 小于;曲图l可知,随着温度升高,K1增大,则△H1>0,根据盖斯定律又得△H3=△H1+△H2,所以△H2<△H3; 
【解析】(1)由于M和Z的相对原子质量之比为3:5,故设M和Z的相对原子质量分别为3x,5x,
由于MCO3ZCO3中MCO3和ZCO3的物质的量之比为1:1,故得到的氧化物中MO和ZO的物质的量之比也为1:1,根据MCO3ZCO3的质量为1.84g,得到氧化物的质量为0.96g,可得: ![]() =
=![]() ,解得:x=8,M的相对原子质量为3x=24,故M为Mg,Z的相对原子质量为5x=40,故Z为Ca,则矿石的化学式为MgCO3CaCO3,故答案为:MgCO3CaCO3;
,解得:x=8,M的相对原子质量为3x=24,故M为Mg,Z的相对原子质量为5x=40,故Z为Ca,则矿石的化学式为MgCO3CaCO3,故答案为:MgCO3CaCO3;
(2)①由于灼烧后的产物为CaO和MgO的混合物,而真空高温条件下用单质硅还原,仅得到单质Mg和一种含氧酸盐,由于此含氧酸盐中只含Z、Si和O元素,且Z和Si的物质的量之比为2:1,故为Ca2SiO4,故此反应的化学方程式为:2MgO+2CaO+Si![]() 2Mg+Ca2SiO4,故答案为:2MgO+2CaO+Si
2Mg+Ca2SiO4,故答案为:2MgO+2CaO+Si![]() 2Mg+Ca2SiO4;
2Mg+Ca2SiO4;
②溶液中含有的阳离子的放电顺序为:H+>Mg2+,阴离子的放电顺序为:Cl->OH-,电解MgCl2溶液时,阴极上H+比Mg2+容易得到电子,电极反应式为2H2O+2e-=H2↑+2OH-,所以得不到镁单质,故答案为:电解MgCl2溶液时,阴极上H+比Mg2+容易得到电子,电极反应式为2H2O+2e-=H2↑+2OH-,所以得不到镁单质;
(3)由图l可知,随着温度升高,K1增大,则反应1:CO2(g)+H2(g)CO(g)+H2O(g)△H1>0,反应3由反应1+2所得,根据盖斯定律:△H3=△H1+△H2,所以△H2<△H3,故答案为:小于;曲图l可知,随着温度升高,K1增大,则△H1>0,根据盖斯定律又得△H3=△H1+△H2,所以△H2<△H3;
(4)由图l可知,随着温度升高,K3减小,则反应3CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H3<0,t时刻迅速降温到T2,降低温度平衡向正反应方向移动,CH3OH浓度增大,t时刻后甲醇浓度随时间变化至平衡的示意曲线为: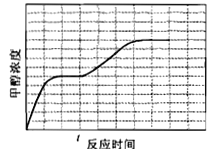 ,故答案为:
,故答案为: 。
。

 阅读快车系列答案
阅读快车系列答案