题目内容
6.下列反应曾用于检测司机是否酒后驾驶:2Cr2O72-+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
(1)Cr3+基态核外电子排布式为1s22s22p63s23p63d3;配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是O(填元素符号).
(2)CH3COOH中C原子轨道杂化类型为sp3和sp2.
(3)H2O分子的空间构型为V形;H2O与CH3CH3OH可以任意比例互溶,除因为它们都是极性分子外,还因为H2O与CH3CH3OH之间可以形成氢键.
分析 (1)Cr位于周期表第四周期ⅥB族,原子核外电子排布为1s22s22p63s23p63d54s1,失去3个电子生成Cr3+,配合物[Cr(H2O)6]3+中Cr3+为中心离子,H2O为配体;
(2)CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子;
(3)H2O中心原子O原子价层电子对为2+2=4,VSEPR模型为四面体,由于含有2对孤电子对,故为V型,H2O与CH3CH3OH都含有氢键,且都为极性分子,二者互溶.
解答 解:(1)Cr位于周期表第四周期ⅥB族,原子核外电子排布为1s22s22p63s23p63d54s1,失去3个电子生成Cr3+,则离子的电子排布为1s22s22p63s23p63d3,
配合物[Cr(H2O)6]3+中Cr3+为中心离子,H2O为配体,O原子提供孤对电子,与Cr3+形成配位键,
故答案为:1s22s22p63s23p63d3;O;
(2)CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子,分别为sp3杂化、sp2杂化,
故答案为:sp3和sp2;
(3)H2O中心原子O原子价层电子对为2+2=4,VSEPR模型为四面体,由于含有2对孤电子对,故为V型,H2O与CH3CH3OH都含有氢键,且都为极性分子,二者互溶,
故答案为:V型;H2O与CH3CH3OH之间可以形成氢键.
点评 本题综合考查原子结构与元素的性质,题目涉及核外电子排布、杂化类型以及等问题,侧重于学生的分析能力的考查,注意把握相关知识的判断方法,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.某饱和醇1mol与O2气充分燃烧产生标况下44.8L的CO2气体,另取1mol该醇与足量的Na反应,收集到标况下22.4L的气体,则该醇为( )
| A. | CH4O | B. | CH3CH2OH | C. |  | D. | 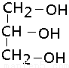 |
1.以下有关物质的量浓度的叙述正确的是( )
| A. | 等体积硫酸铁、硫酸铜、硫酸钾溶液分别与足量的氯化钡溶液反应,若生成的硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐溶液的物质的量浓度比为1:2:3 | |
| B. | 150 mL 1mol•L-1的氯化钾溶液中的c(Cl-)与50 mL 1 mol•L-1的氯化铝溶液中的c(Cl-) 相等 | |
| C. | 20℃时,饱和KCl溶液的密度为1.174g•cm-3,物质的量浓度为4.0 mol•L-1,则此溶液中KCl 的质量分数为25.38% | |
| D. | 20℃时,100 g水可溶解34.2g KCl,此时KCl饱和溶液的质量分数为34.2% |
11.苯丙酸诺龙是一种兴奋剂,结构简式为有关苯丙酸诺龙的说法不正确的是( )
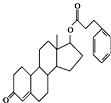

| A. | 含有两种官能团 | B. | 含有脂环 | ||
| C. | 是一种芳香化合物 | D. | 含有酯基 |
18.A、B、C、D四种元素在周期表中分别处于元素X的四周(如图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它们所处的同族中最小的.试确定:
(1)各元素的符号:A:Si,B:N,C:S,X:P.
(2)画出C元素的简单阴离子的结构示意图: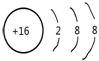
(3)C、D、X最高价氧化物对应水化物酸性由强到弱的顺序:C>X>D(用C、D、X表示).
(4)把A、B、X气态氢化物按照稳定性由强到弱的顺序排列:SiH4<PH3<NH3(用化学式表示).
附加题:A、B、C、D是原子序数小于20的四种元素,已知A元素+1价的阳离子与B、D的阴离子具有相同的电子层结构,B元素最高正价与负价的绝对值之差等于6.1mol C单质与足量的稀硫酸反应可生成1.5mol H2,反应后C元素原子形成的离子和氖原子的电子层结构相同.D元素原子的最外层电子数是C元素原子的最外层电子数的2倍.试回答:
(1)A、B、C、D四种元素依次是钾、氯、铝、硫(写出元素名称).
(2)写出A与C、B与D最高价氧化物的水化物的化学式(按酸性或碱性由强至弱的顺序)碱性:KOH>Al(OH)3,酸性:HClO4>H2SO4.
(3)写出A、C两元素最高价氧化物的水化物间反应的化学方程式Al(OH)3+OH-=AlO2-+2H2O.
| B | ||
| A | X | C |
| D |
(2)画出C元素的简单阴离子的结构示意图:
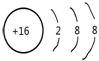
(3)C、D、X最高价氧化物对应水化物酸性由强到弱的顺序:C>X>D(用C、D、X表示).
(4)把A、B、X气态氢化物按照稳定性由强到弱的顺序排列:SiH4<PH3<NH3(用化学式表示).
附加题:A、B、C、D是原子序数小于20的四种元素,已知A元素+1价的阳离子与B、D的阴离子具有相同的电子层结构,B元素最高正价与负价的绝对值之差等于6.1mol C单质与足量的稀硫酸反应可生成1.5mol H2,反应后C元素原子形成的离子和氖原子的电子层结构相同.D元素原子的最外层电子数是C元素原子的最外层电子数的2倍.试回答:
(1)A、B、C、D四种元素依次是钾、氯、铝、硫(写出元素名称).
(2)写出A与C、B与D最高价氧化物的水化物的化学式(按酸性或碱性由强至弱的顺序)碱性:KOH>Al(OH)3,酸性:HClO4>H2SO4.
(3)写出A、C两元素最高价氧化物的水化物间反应的化学方程式Al(OH)3+OH-=AlO2-+2H2O.
15.下列说法正确的是( )
| A. | 向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色 | |
| B. | 欲除去Cl2中少量HCl气体,可将此混合气体通过盛饱和食盐水的洗气瓶 | |
| C. | 漂白粉的有效成分是CaCl2和Ca(ClO)2,应密闭保存 | |
| D. | 氯气有漂白性,所以氯气能使有色布条褪色 |

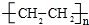 ,该反应属于加聚反应;
,该反应属于加聚反应; +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$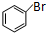 +HBr.
+HBr.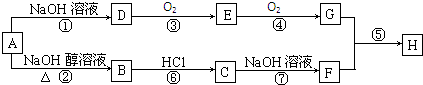
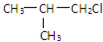 ,G的官能团名称是羧基
,G的官能团名称是羧基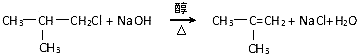 ;E与新制Cu(OH)2反应:
;E与新制Cu(OH)2反应: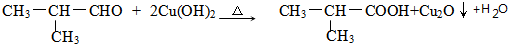 .
.