题目内容
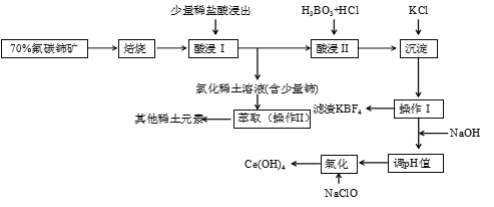
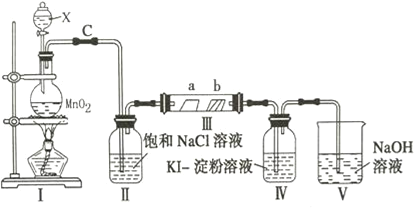
【题目】X是合成一种新型抗肝炎药的中间体,其生产路线如下:
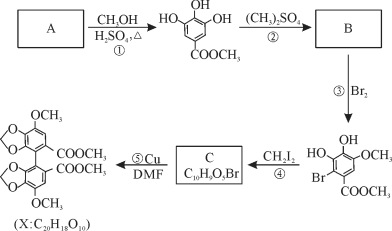
回答下列问题:
(1)反应①的反应类型为_____________。
(2)反应③的化学方程式为____________________________________________________。
(3)反应④生成C的结构简式为______________________,无机产物为_____(填化学式)。
(4)A有多种同分异构体,同时符合下列条件的有______种(不考虑立体异构)。请写出其中一种核磁共振氢谱有4组峰,且峰面积之比为2∶2∶1∶1的结构简式___________。
a.苯环上有4个取代基;
b.与FeCl3溶液发生显色反应;
c.能发生水解反应。
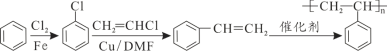
(5)参照上述合成路线及信息,以氯气、苯和一氯乙烯为原料(其它试剂任选),设计制备聚苯乙烯的合成路线____________________________________________________。
【答案】取代反应(酯化反应) 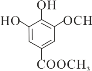 +Br2→
+Br2→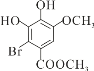 + HBr
+ HBr 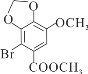 HI 6
HI 6 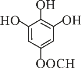 或
或 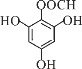
【解析】
由已知结合流程可得,A: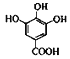 与CH3OH发生①酯化反应(取代反应),生成
与CH3OH发生①酯化反应(取代反应),生成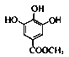 ;
; 与(CH3)2SO4发生②取代反应,生成B:
与(CH3)2SO4发生②取代反应,生成B: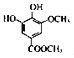 ;
; 与Br2发生③取代反应,生成
与Br2发生③取代反应,生成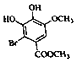 ;
; 与CH2I2发生④取代反应,生成C:
与CH2I2发生④取代反应,生成C: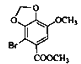 ;两分子
;两分子 发生⑤取代反应,生成联苯双酯
发生⑤取代反应,生成联苯双酯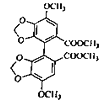 。
。
(1)由以上分析可知, 与CH3OH发生①的反应类型为酯化反应(取代反应),
与CH3OH发生①的反应类型为酯化反应(取代反应),
故答案为:取代反应(酯化反应);
(2)反应③为 与Br2发生取代反应,生成
与Br2发生取代反应,生成 和HBr,化学方程式为
和HBr,化学方程式为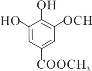 +Br2→
+Br2→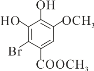 + HBr,
+ HBr,
故答案为: +Br2→
+Br2→ + HBr;
+ HBr;
(3)反应④为 与CH2I2发生取代反应,生成C为:
与CH2I2发生取代反应,生成C为: ,无机产物为HI,
,无机产物为HI,
故答案为: ;HI;
;HI;
(4)A为 ,其同分异构体:“a.苯环上有4个取代基”,“b.与FeCl3溶液发生显色反应”,则必有酚羟基;“c.能发生水解反应”,则含有酯基,综上,符合条件的结构简式为:
,其同分异构体:“a.苯环上有4个取代基”,“b.与FeCl3溶液发生显色反应”,则必有酚羟基;“c.能发生水解反应”,则含有酯基,综上,符合条件的结构简式为: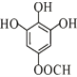 、
、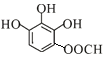 、
、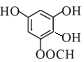 、
、![]() 、
、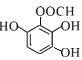 、
、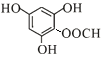 共6种,其中一种核磁共振氢谱有4组峰,且峰面积之比为2∶2∶1∶1的结构简式为:
共6种,其中一种核磁共振氢谱有4组峰,且峰面积之比为2∶2∶1∶1的结构简式为: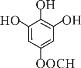 或
或 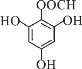 ,
,
故答案为:6; 或
或  ;
;
(5)首先苯和氯气取代生成氯苯,然后氯苯与氯乙烯取代生成苯乙烯,最后苯乙烯发生加聚反应生成聚苯乙烯,合成路线如下: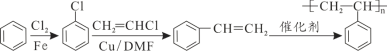 ,
,
故答案为: 。
。

 阅读快车系列答案
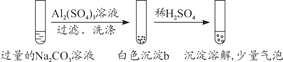
阅读快车系列答案【题目】某学生探究0.25 mol·L-1 Al2(SO4)3溶液与0.5 mol·L-1 Na2CO3溶液的反应,实验如下。下列分析错误的是
实验1 |
|
实验2 |
|
A. 实验1中,白色沉淀a是Al(OH)3
B. 实验2中,白色沉淀b中含有CO![]()
C. 检验白色沉淀a、b是否洗涤干净,不可使用相同的检验试剂
D. 实验1、2中,白色沉淀成分不同可能与混合后溶液的pH有关