题目内容
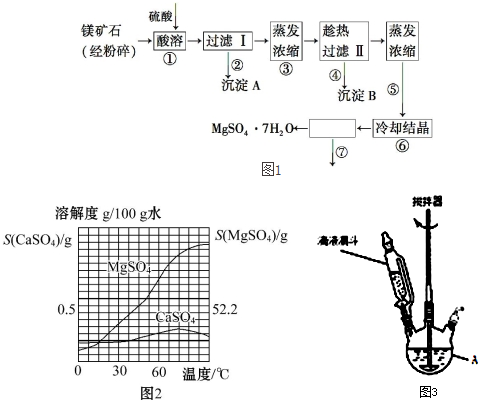
6. (1)某学生课外活动小组利用图1所示装置分别做如下实验:
(1)某学生课外活动小组利用图1所示装置分别做如下实验:①在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是稀氨水和酚酞溶液;加热时溶液由红色逐渐变浅的原因是稀氨水中的NH3气逸出,所以溶液的颜色变浅.
②在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是溶有SO2的品红溶液;加热时溶液由无色变为红色的原因是SO2气体逸出,品红溶液恢复红色.
(2)A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图2所示.
①若A是淡黄色固体:则B是H2S,E是H2SO4.(填化学式)
②若A是无色气体:B→C的化学方程式为4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O.
分析 (1)实验的装置为一封闭体系,受热时,有气体从溶液中逸出进入气球,导致溶液的颜色的变化;冷却后,逸出的气体又溶解在溶液中,得到原来溶液,恢复到原来溶液的颜色.在中学阶段,因为气体的溶入和逸出而导致溶液颜色互变的最常见的是SO2与品红溶液之间以及NH3与酚酞溶液之间,然后根据题中现象进行分析、验证并解答即可;
(2)①如果A是淡黄色固体,A与氧气反应生成C,则A为S,C为SO2,根据题中转化关系,A与氢气反应生成B为H2S,C与氧气反应生成D为SO3,D与水反应生成E为H2SO4,浓硫酸与铜加热条件下反应生成二氧化硫,符合转化关系;
②如果A是无色气体,根据题中转化关系,A能与氢气也能和氧反应,则A应为N2,B为NH3,C为NO,D为NO2,E为HNO3,铜与稀硝酸反应生成一氧化氮,符合转化关系,据此答题;
解答 解:(1)①因稀氨水呈碱性能使酚酞变红,同时氨水不稳定易分解,加热氨气逸出,溶液碱性减弱,溶液颜色逐渐变浅,冷却后氨气又溶解,溶液呈碱性,酚酞变红,
故答案为:稀氨水和酚酞;稀氨水中的NH3气逸出,所以溶液的颜色变浅;
②SO2能与品红发生化合反应,生成不稳定的无色物质,使品红褪色,加热时,生成的无色物质不稳定分解,SO2气体逸出,又生成品红,故溶液变为红色,冷却后SO2又使品红溶液褪色,
故答案为:溶有SO2的品红;SO2气体逸出,品红溶液恢复红色;
(2)①如果A是淡黄色固体,A与氧气反应生成C,则A为S,C为SO2,根据题中转化关系,A与氢气反应生成B为H2S,C与氧气反应生成D为SO3,D与水反应生成E为H2SO4,浓硫酸与铜加热条件下反应生成二氧化硫,E→C的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑,
故答案为:H2S;H2SO4;
(2)如果A是无色气体,根据题中转化关系,A能与氢气也能和氧反应,则A应为N2,B为NH3,C为NO,D为NO2,E为HNO3,铜与稀硝酸反应生成一氧化氮,符合转化关系,B→C的化学方程式为4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6 H2O,
故答案为:4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6 H2O
点评 本题考查框图推断,主要考查硫、氮的单质及其化合物知识,学生由实验现象判定实验原理的逆向思维能力等,解题的关键是在审题的基础上找准解题的突破口,经过分析,归纳,推理,得出正确的答案,难度中等,旨在考查学生对基础知识的掌握熟练程度,注意基础的全面掌握.

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案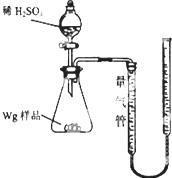 用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为amL,实验后量气管的最终读数为bmL.请回答下列问题:
用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为amL,实验后量气管的最终读数为bmL.请回答下列问题:(1)按如图完成装置连接,开始实验前必须进行的操作是检查装置的气密性.具体方法是将导气管插到液面以下,用双手握住锥形瓶外壁(或用热毛巾加热试管),导气管口有气泡冒出,则说明气密性良好,无气泡则说明漏气或松开双手,看导管口能否形成一段水柱,若形成一段水柱,则装置的气密性良好,否则说明漏气.
(2)写出锥形瓶中发生化合反应的离子方程式:2Fe3++Fe=3Fe2+.
(3)实验结束后,锥形瓶内溶液中存在的金属离子有哪些可能?请根据选项进行填空(表格不一定填完):
A.盐酸 B.KSCN溶液 C.酸性KMnO4溶液 D.H2O2溶液
| 序号 | 溶液中可能存在的金属离子 | 选择最少种数的试剂,验证该假设(填字母) |
| ① | ||
| ② | ||
| ③ |
(5)若样品与足量稀硫酸反应后滴入KSCN溶液不显红色且量气管读数b>a(该实验条件下 的气体摩尔体积为Vm).下列有关单质铁质量分数的计算过程是否正确?否(填“是”或“否”),理由是混合物中Fe2O3与硫酸反应后生成的Fe3+可进一步消耗铁单质.
| A. | 苏打溶液与稀盐酸反应的离子反应方程式:HCO3-+H+═CO2↑+H2O | |
| B. | Fe2O3与HI:Fe2O3+6H+═2Fe3++3H2O | |
| C. | NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 浓烧碱溶液中加入铝片:Al+OH-+H2O═AlO2-+H2↑ |
| A. | 闻名世界的中国陶瓷、酿酒、造纸技术都充分应用了化学工艺 | |
| B. | 四大发明之一黑火药是由硫黄、硝石、木炭三种物质按一定比例混合制成 | |
| C. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| D. | 由于中国大部分地区都缺碘,而缺碘就会引起碘缺乏病,80年代国家强制给食用的氯化钠食盐中加入碘单质 |