题目内容
9.准确配制一定物质的量浓度的NaOH溶液,下面实验操作中不正确的是( )| A. | 用托盘天平称量时,应将NaOH固体放在小烧杯或玻璃器皿中 | |
| B. | 将烧杯中未冷却的NaOH溶液直接注入未经干燥的容量瓶中 | |
| C. | 定容时视线应平视凹液面(或平视刻度线),直到凹液面的最低点与刻度线相切 | |
| D. | 将称好的NaOH固体放入烧杯中,加入适量水溶解 |
分析 A、药品不能直接放在天平左盘内进行称量;
B、溶液配制不能在容量瓶内进行溶解或稀释,溶解或稀释会产生热化学,影响溶液体积,甚至会导致容量瓶破裂的危险;
C、定容时视线应平视凹液面,直到凹液面的最低点与刻度线水平相切;
D、将称好的NaOH固体,先放在烧杯里溶解,然后再移入容量瓶.
解答 解:A、药品不能直接放在天平左盘内进行称量,氢氧化钠具有腐蚀性且易水解,通常放置在烧杯内迅速称量,故A正确;
B、溶液配制不能在容量瓶内进行溶解或稀释,溶解或稀释会产生热化学,影响溶液体积,甚至会导致容量瓶破裂的危险,故应向将称好的NaOH固体放入烧杯中,加入少量水溶解,恢复室温后再移入容量瓶,故B错误;
C、定容时视线应平视凹液面,直到凹液面的最低点与刻度线水平相切,故C正确;
D、将称好的NaOH固体放入烧杯中,加入适量水溶解,然后再移入容量瓶,故D正确;
故选B.
点评 本题考查天平的使用、溶液配制的基本操作,难度不大,注意基础知识的掌握.

练习册系列答案
相关题目
4.在钢铁的生锈过程中(吸氧腐蚀)可能发生的反应是( )
| A. | 4Fe+3O2═2Fe2O3 | B. | O2+4e-+2H2O═4OH- | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | Fe+2H+═Fe2++H2↑ |
14.下列化学用语正确的是( )
| A. | 硫的原子结构示意图: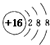 | |
| B. | NH4Br的电子式: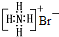 | |
| C. | Be2+离子中的质子数和电子数之比为2:1 | |
| D. | 中子数为146、原子序数为92的铀(U)原子:${\;}_{92}^{146}$U |
11.下列说法不正确的是( )
| A. | 利用蓝绿藻等低等植物和微生物在阳光作用下使水分解产生氢气,该方法符合绿色化学原则 | |
| B. | 12C、13C和14C互为同位素,它们的放射性可用于考古断代,可测定生物体死亡的年代 | |
| C. | 超高分辨荧光显微镜可以观察到纳米世界,其中利用了荧光蛋白,生物发光也与荧光蛋白有关,生物发光是将化学能转化为光能的过程 | |
| D. | 分子筛中有许多笼状空穴和通道可用于分离、提纯气体,还可用作干燥剂、离子交换剂、催化剂和催化剂载体 |
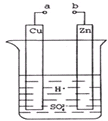 原电池是化学对人类的一个重大贡献.
原电池是化学对人类的一个重大贡献.