题目内容
20.NA代表阿伏伽德罗常数的数值,下列说法中正确的是( )| A. | 1mol铁完全反应,一定失去2NA个电子 | |
| B. | 1mol任何物质都约含6.02×1023个分子 | |
| C. | 等物质的量的NO和NO2含的N原子数均为1mol | |
| D. | 标况下,22.4L氦气所含的原子总数为NA |
分析 A、铁有+2和+3价两个价态;
B、物质不一定由分子构成;
C、NO和NO2中均含1个N原子;
D、氦气为单原子分子.
解答 解:A、铁有+2和+3价两个价态,故反应后1mol铁可能失去2mol或3mol电子,即失去的可能为2NA个也可能为3NA个电子,故A错误;
B、物质不一定由分子构成,可能由原子或离子构成,故B错误;
C、NO和NO2中均含1个N原子,故等物质的量的NO和NO2含的N原子的物质的量相等,但不一定是1mol,故C错误;
D、标况下,22.4L氦气的物质的量为1mol,而氦气为单原子分子,故1mol氦气中含1mol原子即NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
11.已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是( )
| A. | 原子半径:A>B>C>D | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D>C>B>A | D. | 金属性:B>A,非金属性:D>C |
15.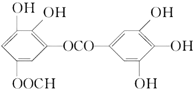 某有机物的结构简式是(如图),下列关于它的性质叙述正确的是( )
某有机物的结构简式是(如图),下列关于它的性质叙述正确的是( )
①能发生加成反应
②能溶解于NaOH溶液
③能水解生成两种酸
④不能因发生加成反应而使溴水褪色
⑤能发生酯化反应
⑥有酸性.
 某有机物的结构简式是(如图),下列关于它的性质叙述正确的是( )
某有机物的结构简式是(如图),下列关于它的性质叙述正确的是( )①能发生加成反应
②能溶解于NaOH溶液
③能水解生成两种酸
④不能因发生加成反应而使溴水褪色
⑤能发生酯化反应
⑥有酸性.
| A. | ①②③ | B. | ②③⑤ | C. | ⑥ | D. | 全部正确 |
5.a、b、c、d是HCl、BaCl2、AgNO3、Na2CO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
由上述现象可推知a、b、c、d依次是( )
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
| A. | AgNO3、HCl、Na2CO3、BaCl2 | B. | AgNO3、HCl、BaCl2、Na2CO3 | ||
| C. | BaCl2、Na2CO3、AgNO3、HCl | D. | HCl、BaCl2、AgNO3、Na2CO3 |
9.卤代烃Y的相对分子质量为92.5,取0.1molY与足量NaOH溶液共热后,再稀HNO3酸化,加入足量AgNO3溶液,得白色沉淀14.35g,则Y与NaOH的乙醇溶液共热,反应后生成的不饱和烃有( )种.
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
10.下列对一些实验事实和理论解释正确的是( )
| 选项 | 实验事实 | 理论解释 |
| A | HCl气体溶于水,能导电 | HCl为离子化合物 |
| B | HBr的酸性强于HCl的酸性 | Br的非金属性比Cl强 |
| C | K3C60在熔融状态下能够导电 | K3C60中含有离子键 |
| D | HF的沸点高于HCl | HF分子间形成有氢键 |
| A. | A | B. | B | C. | C | D. | D |
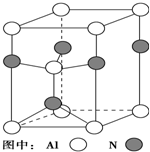 元素周期表中的第ⅢA、ⅣA、ⅤA族的部分元素往往易形成原子晶体,氮化铝、氮化硼、磷化硼和砷化镓属于此列,如氮化铝晶体晶胞如右图所示
元素周期表中的第ⅢA、ⅣA、ⅤA族的部分元素往往易形成原子晶体,氮化铝、氮化硼、磷化硼和砷化镓属于此列,如氮化铝晶体晶胞如右图所示