题目内容
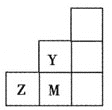
【题目】如图所示为元素周期表中短周期的一部分,下列关于Y、Z、M的说法正确的是 ( )
A.电负性:![]()
B.离子半径:![]()
C.![]() 分子中各原子的最外层均满足8电子稳定结构
分子中各原子的最外层均满足8电子稳定结构
D.Z元素基态原子的最外层电子排布图为![]()
【答案】C
【解析】
由短周期元素在周期表中的位置可知,Y为F,Z为S,M为Cl。
A.一般来说,同周期元素从左到右,电负性逐渐增强,则电负性:![]() ,故A错误;
,故A错误;
B.![]() 、
、![]() 、
、![]() 分别为
分别为![]() 、
、![]() 、
、![]() ,其中
,其中![]() 的核外电子层最少,所以半径最小,
的核外电子层最少,所以半径最小,![]() 和
和![]() 的核外电子层结构相同,根据具有相同电子层结构的离子,核电荷数越大离子半径越小,可知离子半径:
的核外电子层结构相同,根据具有相同电子层结构的离子,核电荷数越大离子半径越小,可知离子半径:![]() ,故B错误;
,故B错误;
C.![]() 为
为![]() ,S的最外层电子数为6,Cl的最外层电子数为7,S和Cl各形成两对共用电子对,其分子中S和Cl的最外层均满足8电子稳定结构,故C正确;
,S的最外层电子数为6,Cl的最外层电子数为7,S和Cl各形成两对共用电子对,其分子中S和Cl的最外层均满足8电子稳定结构,故C正确;
D.题给电子排布图违反泡利原理,同一原子轨道中的2个电子自旋状态应相反,故D错误;
答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】有Ⅰ~Ⅳ四个体积均为0.5 L的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入HCl和O2(如下表),加入催化剂发生反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
容器 | 起始时 | ||
t/℃ | n(HCl)/mol | Z | |
Ⅰ | 300 | 0.25 | a |
Ⅱ | 300 | 0.25 | b |
Ⅲ | 300 | 0.25 | 4 |

A. ΔH<0,a<4<b
B. 300℃该反应的平衡常数的值为64
C. 容器Ⅲ某时刻处在R点,则R点的υ正>υ逆,压强:p(R)>p(Q)
D. 若起始时,在容器Ⅳ中充入0.25molCl2和0.25molH2O(g),300℃达平衡时容器中c(HCl)=0.1mol·L-1



