题目内容
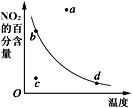
【题目】如图是某条件时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )

A.该反应的热化学方程式为:2NH3N2+3H2△H=﹣92kJ·mol﹣1
B.生成物的能量之和比反应物的能量之和高 92 kJ
C.a曲线是未加入催化剂时的能量变化曲线
D.加入催化剂可增加正反应速率,减小逆反应速率
【答案】C
【解析】
A.该反应的热化学方程式为:N2(g)+3H2(g)2NH3(g)△H=﹣92kJ/mol,故A错误;
B.依据图象可知,反应物的能量之和比生成物的能量之和高92kJ,故B错误;
C.催化剂降低反应的活化能,改变反应速率不改变平衡,a曲线是未加入催化剂时的能量变化曲线,b曲线是加入催化剂时的能量变化曲线,故C正确;
D.加入催化剂可同等程度增加正逆反应速率,故D错误;
故选:C。

练习册系列答案
相关题目