题目内容
9.下列表示方法正确的是( )①乙烯的结构简式:CH2CH2
②NH4Cl电子式:
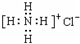
③苯乙醛结构简式:
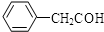
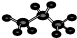
④丙烷分子的球棍模型
| A. | ①④ | B. | ②④ | C. | ④ | D. | ②③ |
分析 ①烯、炔的结构简式碳碳双键、碳碳三键不能省略;
②氯化铵为离子化合物,铵根离子和氯离子都需要标出所带电荷及最外层电子;
③苯乙醛的结构简式中醛基书写错误;
④丙烷分子中含有两个甲基、1个亚甲基,据此判断其球棍模型.
解答 解:①乙烯分子中含有碳碳双键,乙烯正确的结构简式为:CH2═CH2,故①错误;
②氯化铵是离子化合物,由氨根离子与氯离子构成,氯离子需要标出最外层电子,正确的电子式为: ,故②错误;
,故②错误;
③苯乙醛的结构简式中醛基书写错误,苯乙醛的结构简式为: ,故③错误;
,故③错误;
④丙烷分子中含有两个甲基和1个亚甲基,碳原子半径大于氢离子,则丙烷的球棍模型为 ,故④正确;
,故④正确;
故选C.
点评 本题考查了电子式的书写方法判断,题目难度中等,注意掌握常见化学用语的概念及书写原则,明确离子化合物与共价化合物的电子式的表示方法及区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.已知去甲肾上腺素可以调控动物机体的植物性神经功能,其结构简式如图所示.下列说法正确的是( )
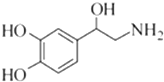

| A. | 去甲肾上腺素的分子式为C8H10O3N | |
| B. | 既能与FeCl3发生显色反应,也能和Na2CO3反应 | |
| C. | 1mol去甲肾上腺素最多能与2mol Br2发生取代反应 | |
| D. | 核磁共振氢谱显示应该有8种不同的氢原子. |
20.将0.5mol SO2(g)和0.3mol O2(g)放入容积为10L的密闭容器中,反应2SO2(g)+O2(g)?2SO3(g)在一定条件下达到平衡时测得n(SO3)=0.4mol,则该条件下反应的平衡常数K为( )
| A. | 160 | B. | 160mol-1 | C. | 1600mol•L-1 | D. | 1600L•mol-1 |
4.下列各组物质间,一定互为同系物的是( )
| A. | C2H6O和C4H10O | B. | C3H6O2和C4H8O2 | C. | C4H10和C10H22 | D. | C3H4和C4H6 |
14.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,2.24 L CCl4所含的原子数为0.5 NA | |
| B. | 标准状况下0.5mol NO和0.5mol O2组成的混合气体的体积约为22.4L | |
| C. | 78 g Na2O2 与足量水反应转移电子数为NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1 NA |
 .
. .
. 氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.
氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.