题目内容
1.A、B、C、D为中学常见物质且均含有同一种短周期元素,相互转化关系如图(反应条件及其它物质已经略去):A$\stackrel{+O_{2}}{→}$B$\stackrel{+O_{2}}{→}$C$\stackrel{+H_{2}O}{→}$D(1)若A、B、C、D的水溶液均能使紫色石蕊试液变红.写出B→C的化学方程式:2SO2+O2$?_{△}^{催化剂}$2SO3
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红.写出A→B的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(3)若A为单质,组成元素的原子序数是其周期序数的3倍,写出相互转化关系图中C的电子式:
 .
.
分析 A、B、C、D为中学常见物质且均含有同一种元素,根据题中各物质转化关系,A能经过两步氧化得C,C与水反应生成D,
(1)若A、B、C、D均为化合物,而且它们的水溶液均能使湿润的蓝色石蕊试纸变红,它们的水溶液均呈酸性,则A为H2S,B为SO2,C为SO3,D为H2SO4;
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,则A为NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,D呈酸性,则B为NO,C为NO2,D为HNO3;
(3)若A为单质,组成元素的原子序数是其周期序数的3倍,则原子序数为6,为C元素,位于周期表第二周期ⅣA族元素,B为CO,C为CO2,D为H2CO3.
解答 解:A、B、C、D为中学常见物质且均含有同一种元素,根据题中各物质转化关系,A能经过两步氧化得C,C与水反应生成D,
(1)若A、B、C、D均为化合物,而且它们的水溶液均能使湿润的蓝色石蕊试纸变红,它们的水溶液均呈酸性,则A为H2S,B为SO2,C为SO3,D为H2SO4,B→C的化学方程式为2SO2+O2$?_{△}^{催化剂}$2SO3 ,故答案为:2SO2+O2$?_{△}^{催化剂}$2SO3 ;
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,则A为NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,D呈酸性,则B为NO,C为NO2,D为HNO3,A→B的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(3)若A为单质,组成元素的原子序数是其周期序数的3倍,则原子序数为6,为C元素,位于周期表第二周期ⅣA族元素,B为CO,C为CO2,D为H2CO3,CO2的电子式为 ,故答案为:
,故答案为: .
.
点评 本题考查无机物的推断,为高频考点,把握转化中的连续氧化及两种强酸为推断的关系,侧重N及其化合物、S及其化合物性质的考查,题目难度不大.

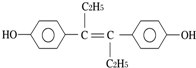
| A. | 可发生聚合反应,不能发生还原反应 | |
| B. | 可与NaOH或NaHCO3发生反应 | |
| C. | 1mol该物质可与5mol Br2发生反应 | |
| D. | 该分子中最多可能有16个碳原子共平面 |
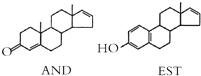
| A. | AND和EST都能使酸性 KMnO4溶液褪色 | |
| B. | AND和EST两者的相对分子质量之差为14 | |
| C. | AND和EST分别与足量氢气加成后的两种生成物互为同系物 | |
| D. | AND和EST与溴水完全反应消耗溴单质的物质的量之比为2:3 |
| A. | 鉴别AgNO3溶液和BaCl2溶液 | B. | 检验鸡蛋壳(CaCO3)能否溶于酸 | ||
| C. | 检验自来水中是否含Cl- | D. | 除去热水瓶内壁上的水垢 |
| A. | 次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| B. | 硫酸亚铁溶液中加过氧化氢溶液 Fe2++2H2O2+4H+═Fe3++4H2O | |
| C. | 用氨水吸收少量二氧化硫 2NH3.H2O+SO2═2NH4++SO32-+H2O | |
| D. | 硝酸铁溶液中加过量氨水 Fe3++3NH3.H2O═Fe(OH)3↓+3NH4+ |
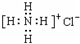
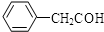
 )化合物:
)化合物:
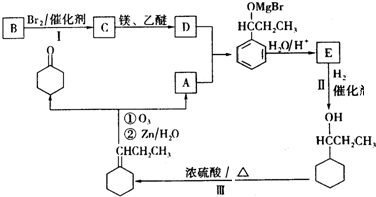
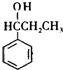 .
.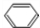 +Br2$\stackrel{催化剂}{→}$
+Br2$\stackrel{催化剂}{→}$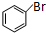 +HBr.
+HBr.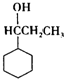 .
.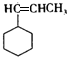 .F在一定条件下发生加聚反应的化学方程式是n
.F在一定条件下发生加聚反应的化学方程式是n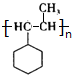 .
.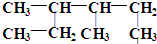 的名称为3,4-二甲基己烷,它的一氯代物有4种同分异构体.
的名称为3,4-二甲基己烷,它的一氯代物有4种同分异构体.