题目内容
【题目】下列关于四个图象的说法正确的是( ) 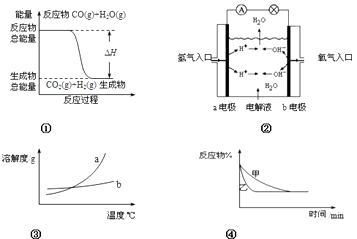
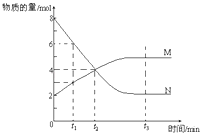
A.图①表示化学反应中能量的变化,反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H>0
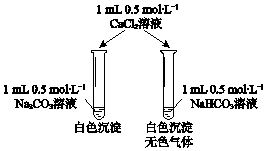
B.图②为氢氧燃料电池示意图,正、负极通入的气体体积之比为2:1
C.图③表示物质a、b的溶解度曲线,可以用结晶方法从a、b混合物中提纯a
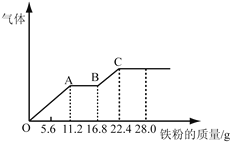
D.图④可以表示压强对可逆反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响,且乙的压强大
3C(g)+D(s)的影响,且乙的压强大
【答案】C
【解析】解、A、因反应物的总能量>生成物的总能量,根据能量守恒原理,该反应为放热,△H<0,故A错误;
B、因氢氧燃料电池的总反应:2H2+O2=2H2O,负极放电的物质为H2 , 正极放电的物质为O2 , 两者的物质的量之比为2,故B错误;
C、因物质a的溶解度随温度变化较大,而物质b的溶解度随温度变化不大,因此,可以用降温结晶方法从a、b混合物中析出物质a,故C正确;
D、因乙先到达平衡,故乙的压强大,甲的压强小,但增大压强,平衡向正反应方向移动,而图象中平衡未发生移动,乙应是加入催化剂的原因,故D错误;
故选:C.
【考点精析】关于本题考查的溶解度、饱和溶液的概念,需要了解在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫作这种溶质的饱和溶液;还能继续溶解某种溶质的溶液,叫作不饱和溶液;在一定温度下,某固体物质在100克溶剂里达到饱和状态时所溶解的质量,叫作这种物质在这种物质在这种溶剂里的溶解度才能得出正确答案.

 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案【题目】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应的措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1)实验测得,5g甲醇(CH3OH,液态)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式: .
(2)已知化学键的键能为:
化学键 | H﹣H | N﹣H | N≡N |
键能/kJmol﹣1 | 436 | 391 | 945 |
又知反应N2(g)+3H2(g)2NH3(g)△H=a kJmol﹣1 . 试根据表中所列键能数据估算a的值为 .
(3)已知:C(s,石墨)+O2(g)═CO2(g)△H=﹣393kJmol﹣1
2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2599kJmol﹣1
根据盖斯定律,计算 298K时C(s,石墨)和H2(g)反应生成1mol C2H2(g)的焓变为 .