题目内容
6.在120℃的条件下,总质量为2.1g的CO与H2的混合气体在足量的O2中充分燃烧,然后通过足量的Na2O2固体,固体增加的质量为( )| A. | 7.2 g | B. | 4.2 g | C. | 3.6 g | D. | 2.1 g |
分析 CO在氧气中完全燃烧生成CO2,CO2和再与Na2O2反应,方程式为2CO+O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2、2CO2+2Na2O2=2Na2CO3+O2,总方程式为:CO+Na2O2=Na2CO3,可知过氧化钠增重为CO的质量;
H2在氧气中完全燃烧生成H2O,H2O再与Na2O2反应,方程式为2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O、2H2O+2Na2O2=4NaOH+O2,总反应方程式为:H2+Na2O2=2NaOH,可知反应后固体质量增加为氢气质量,以此解答该题.
解答 解:CO在氧气中完全燃烧生成CO2,CO2和再与Na2O2反应,方程式为2CO+O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2、2CO2+2Na2O2=2Na2CO3+O2,总方程式为:CO+Na2O2=Na2CO3,可知过氧化钠增重为CO的质量;
H2在氧气中完全燃烧生成H2O,H2O再与Na2O2反应,方程式为2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O、2H2O+2Na2O2=4NaOH+O2,总反应方程式为:H2+Na2O2=2NaOH,可知反应后固体质量增加为氢气质量,
故由2.1gCO和H2组成的混合物在足量的O2中充分燃烧,立即通入足量的Na2O2固体,固体质量增加应为CO和H2的质量,即固体增重为2.1g,
故选D.
点评 本题考查混合物计算,侧重于学生的分析能力和计算能力的考查,注意利用总反应方程式判断固体增重,也可以利用差量法进行判断,若物质可以写成(CO)x.yH2形式,完全燃烧后通入足量过氧化钠,过氧化钠增重为该物质的质量,难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 18O2-结构示意图: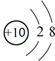 | |
| B. | Na2O2的电子式: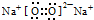 | |
| C. | HCO3- 的水解方程式HCO3-+H2O?H2CO3+OH- | |
| D. | HI的电离方程式 HI?H++I- |
| A. | 标准状况下,22.4L庚烷所含有的分子数为NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 标准状况下,CH4和C2H4的混合气体22.4L,所含的分子数为约为NA | |
| D. | 26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
(1)写出瓦斯爆炸的化学方程式CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O.
(2)可燃性气体的爆炸都有一个爆炸极限,所谓爆炸极限是指可燃气体(或蒸汽或粉尘等)与空气混合后,遇火产生爆炸的最高或最低浓度(通常以体积百分数表示).下表是甲烷在空气和纯氧气中的爆炸极限.
| 空气中 | 纯氧气中 | |
| 甲烷的爆炸极限 | 5.0~15% | 5.0~60% |
A.3% B.10% C.30% D.60%
(3)由矿井中的瓦斯爆炸,根据你的化学实验经验,你可以得出什么启示?(提示:对可燃性气体的加热、点燃操作应该注意的问题)可燃性气体的加热、点燃操作前必须进行验纯操作.
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物稳定性:H2T<H2R | B. | 单质与稀盐酸反应的速率为L<Q | ||
| C. | M与T形成的化合物具有两性 | D. | L2+与R2-具有相同的电子层结构 |
| A. | 上述反应中NO2- 是氧化剂 | |
| B. | 反应过程中溶液的pH增大 | |
| C. | 该反应可以说明氧化性NO3->MnO4- | |
| D. | 上述反应中,1 mol KMnO4可以消耗2.5 mol NaNO2 |
| A. | 滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、SCN- | |
| B. | pH为1的溶液:Fe2+、K+、ClO-、Cl- | |
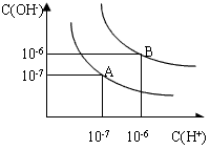
| C. | c(H+)=10-12 mol•L-1的溶液:K+、Ba2+、Cl-、NO3- | |
| D. | 存在较多的H+、SO42-、NO3-的溶液:Al3+、CH3COO-、Cl- |