题目内容
14.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )| A. | 标准状况下,22.4L庚烷所含有的分子数为NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 标准状况下,CH4和C2H4的混合气体22.4L,所含的分子数为约为NA | |
| D. | 26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
分析 A.气体摩尔体积适用对象为气体;
B.甲基是甲烷失去一个H原子后剩余的部分,其中化学键表示一个未成对电子;
C.气体摩尔体积适用单一气体和混合气体;
D.C2H2和苯蒸气的混合气体最简式相同为CH,计算26gCH中含原子数.
解答 解:A.标况下庚烷为液体,不能使用气体摩尔体积,故A错误;
B.甲基是甲烷失去一个H原子后剩余的部分,所以一个甲基中的电子数是9,则1mol甲基(一CH3)所含的电子数应为9mol,故B正确;
C.标准状况下,Vm=22.4/mol,CH4和C2H4的混合气体22.4L,物质的量为1mol,所含的分子数为约为NA,故C正确;
D.C2H2和苯蒸气的混合气体最简式相同为CH,计算26gCH中含原子数=$\frac{26g}{13g/mol}$×1×NA=2NA,故D正确;
故选:A.
点评 本题考查阿伏加德罗常数的应用,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意标况下气体摩尔体积的使用条件,注意甲基的结构,题目难度不大.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
4.下列提纯方法不正确的是( )
| A. | 除去KNO3中的NaCl杂质----结晶 | |
| B. | 除去食盐中的泥沙-----分液 | |
| C. | 除去KCl中的K2CO3-----加适量硝酸 | |
| D. | 除去碘水中的碘-----萃取 |
2.0.4L 1mol/L KCl溶液与0.5L 1mol/L AlCl3溶液中的Cl-的物质的量浓度之比( )
| A. | 15:4 | B. | 3:1 | C. | 4:15 | D. | 1:3 |
9.下列各种液体分别与溴水混合并振荡,静置后混合液分成两层,下层几乎呈无色的是( )
| A. | 苯 | B. | 己烯 | C. | CCl4 | D. | KI |
19.有关于化学实验的操作或者说法中,正确的是( )
| A. | 各种水果之所以有果香味,是因为水果中含有一定的酯类物质 | |
| B. | 苯酚有毒,所以日常所用的药皂中不可能掺入苯酚 | |
| C. | 用浓溴水可以除去苯中少量的苯酚 | |
| D. | 将蔗糖和稀硫酸混合加热后,再加入银氨溶液并水浴加热,以检验还原性糖 |
6.在120℃的条件下,总质量为2.1g的CO与H2的混合气体在足量的O2中充分燃烧,然后通过足量的Na2O2固体,固体增加的质量为( )
| A. | 7.2 g | B. | 4.2 g | C. | 3.6 g | D. | 2.1 g |
3.关于原子结构的叙述中:
①所有原子核均由质子和中子构成;
②原子处于基态时,次外层电子不一定是8个;
③稀有气体元素,其基态原子最外层都是8个电子;
④最外层电子数为2的原子一定是金属原子;
其中正确的是( )
①所有原子核均由质子和中子构成;
②原子处于基态时,次外层电子不一定是8个;
③稀有气体元素,其基态原子最外层都是8个电子;
④最外层电子数为2的原子一定是金属原子;
其中正确的是( )
| A. | ①② | B. | ②③ | C. | 只有② | D. | 只有④ |
4.强碱性溶液中能大量共存的离子组是( )
| A. | Na+、Fe2+、Cl-、SO42- | B. | K+、Ag+、Cl-、NO3- | ||
| C. | Ba2+、Na+、NO3-、CO32- | D. | Na+、K+、CO32-、SO32- |
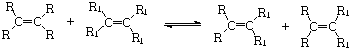
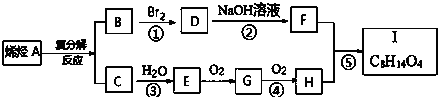
 .
.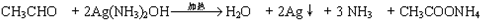 .
.