��Ŀ����
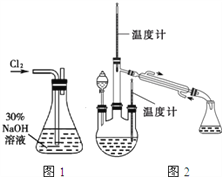
����Ŀ����������(POCl3)�������뵼����Ӽ������άԭ�ϡ�ij��ѧС����PCl3�������Ʊ�POCl3��װ������ͼ��ʾ����֪��POCl3�ķе���105.1�棬PCl3 �ķе���65.5��;��������ʪ������������������
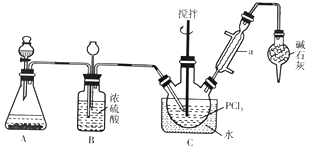
(1)����a������Ϊ_______________��
(2)װ��A�������ķ���װ�ã���д��A�з�����Ӧ�Ļ�ѧ����ʽ��___________________��
(3)װ��B��������______________________________________________________________��
(4)װ��C�з�Ӧ�¶�Ӧ������60��65��,ԭ����_____________________________________��
(5)ͨ��������·����ԲⶨPOCl3��Ʒ����Ԫ�ص�����������ʵ�鲽�����£�
��ȡ1.5000g ��Ʒ����ƿ�У���������NaOH��Һ������ȫˮ����ϡ����������ԡ�
������ƿ�м���3.2000mol��L-1��AgNO3��Һ10.00mL,ʹCl-��ȫ������
�������м���2.00mL������������ҡ����ʹ�������汻���������ǡ�
��������ָʾ������0.2000mol��L-1NH4SCN����Һ�ζ�����Ag+���յ�,����10.00mLNH4SCN��Һ��
��֪��Ksp(AgCl)=3.2��10-10,Ksp(AgSCN)=2.0��10-12��
�ٵζ�ѡ�õ�ָʾ����________(�����)��
a��FeCl2 b��NH4Fe(SO4)2 c������ d������
��ʵ������м�����������Ŀ����_____________________________�����˲���������Ԫ�ص�������������________(�ƫ����ƫС�� ���䡱)��
�۲�Ʒ����Ԫ�ص���������Ϊ_________��
���𰸡� ���������� 2H2O2![]() 2H2O+O2��(��2Na2O2+2H2O=4NaOH+O2��) �۲����������٣���������;ƽ����ѹ �¶ȹ��ͣ���Ӧ����С���¶ȹ���,PCl3�ӷ���Ӱ��POCl3�IJ��� b ��ֹ�ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���� ƫС 71.0%
2H2O+O2��(��2Na2O2+2H2O=4NaOH+O2��) �۲����������٣���������;ƽ����ѹ �¶ȹ��ͣ���Ӧ����С���¶ȹ���,PCl3�ӷ���Ӱ��POCl3�IJ��� b ��ֹ�ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���� ƫС 71.0%
��������(1)�������������֪����a������Ϊ���������ܡ�(2)װ��A�������ķ���װ�ã���Ӧ����Ҫ���ȣ���A�з�����Ӧ�Ļ�ѧ����ʽΪ2H2O2![]() 2H2O+O2����2Na2O2+2H2O��4NaOH+O2����(3)���ɵ������к���ˮ������Ũ�������������ͬʱ����ͨ���۲����ݵ������١����ⳤ��©����������ƽ����ѹ�����á�(4)�����¶ȹ��ͣ���Ӧ����С�����¶ȹ��ߣ�PCl3�ӷ���Ӱ��POCl3�IJ��ʣ�����װ��C�з�Ӧ�¶�Ӧ������60��65�档(5)����������������NH4SCN��Һ��Ӧ�Ժ�ɫ����ζ�ѡ�õ�ָʾ����NH4Fe(SO4)2����ѡb����ʵ������м�����������Ŀ���Ǹ����Ȼ�������ֹAgCl����ת��ΪAgSCN���������ݲ�ȷ�����˲����������ĵ�NH4SCN��Һ�����ƫ�������еļ���ԭ����֪������Ԫ�ص�������������ƫС���۸��������֪��NH4SCN�����ʵ���Ϊ0.002mol������֮��Ӧ�������ӵ����ʵ���Ϊ0.002mol�����ܵ������ӵ����ʵ���Ϊ0.032mol�������������ӷ�Ӧ�������ӵ����ʵ���Ϊ0.032mol��0.002mol��0.03mol�����������ӵ����ʵ���Ϊ0.03mol�����Ʒ��ClԪ�صĺ���Ϊ
2H2O+O2����2Na2O2+2H2O��4NaOH+O2����(3)���ɵ������к���ˮ������Ũ�������������ͬʱ����ͨ���۲����ݵ������١����ⳤ��©����������ƽ����ѹ�����á�(4)�����¶ȹ��ͣ���Ӧ����С�����¶ȹ��ߣ�PCl3�ӷ���Ӱ��POCl3�IJ��ʣ�����װ��C�з�Ӧ�¶�Ӧ������60��65�档(5)����������������NH4SCN��Һ��Ӧ�Ժ�ɫ����ζ�ѡ�õ�ָʾ����NH4Fe(SO4)2����ѡb����ʵ������м�����������Ŀ���Ǹ����Ȼ�������ֹAgCl����ת��ΪAgSCN���������ݲ�ȷ�����˲����������ĵ�NH4SCN��Һ�����ƫ�������еļ���ԭ����֪������Ԫ�ص�������������ƫС���۸��������֪��NH4SCN�����ʵ���Ϊ0.002mol������֮��Ӧ�������ӵ����ʵ���Ϊ0.002mol�����ܵ������ӵ����ʵ���Ϊ0.032mol�������������ӷ�Ӧ�������ӵ����ʵ���Ϊ0.032mol��0.002mol��0.03mol�����������ӵ����ʵ���Ϊ0.03mol�����Ʒ��ClԪ�صĺ���Ϊ![]() ��
��

����Ŀ��H2O2��һ�ֳ����Լ�����ʵ���ҡ���ҵ�������й㷺��;

��.ʵ������H2O2������������ֽ������ܶ�������Ӱ�졣ʵ����70��ʱ��ͬ������H2O2Ũ����ʱ��ı仯����ұ�����ͼ��ʾ��
��1������˵����ȷ���ǣ�________������ĸ��ţ�
A��ͼ�ױ���������������ͬʱ��H2O2Ũ��ԽС����ֽ�����Խ��
B��ͼ�ұ���������������ͬʱ����Һ����Խ����H2O2�ֽ�����Խ��
C��ͼ������������Mn 2+����ʱ����Һ����Խǿ��H2O2�ֽ�����Խ��
D��ͼ����ͼ��������������Һ�У�Mn2+��H2O2�ֽ����ʵ�Ӱ���
��2������Mn2+�ڷ�Ӧ�У��ı���____________________(����ĸ���)
A����Ӧ���� B����Ӧ��C����Ӧ�ʱ� D����Ӧ·��
E.��Ӧ��� F.����Ӱٷ���
��. H2O2�ڹ�ҵ����ΪFenton����Ҫ�Լ��������ڴ������ѽ����л���Ĺ�ҵ��ˮ���ڵ��ں�pH����Һ������ԣ���Fe2+Ũ�ȵķ�ˮ�м���H2O2�����������ǻ����ɻ�������������Ⱦ������ø÷��������л���Ⱦ��p-CP��̽���й����ضԸý��ⷴӦ���ʵ�Ӱ�졣
��ʵ����ơ�����p-CP�ij�ʼŨ����ͬ���㶨ʵ���¶���298K��313K������ʵ���������±�����������¶Ա����飬����ʵ��������ʱ��-p-CPŨ��ͼ���¡�

��3�������Ե��ǻ����ɻ��ĵ���ʽΪ��______________
��4�����������ʵ����Ʊ�(���в�Ҫ���ո�)��
ʵ�� ��� | ʵ��Ŀ�� | T/K | pH | c/10-3mol��L-1 | |
H2O2 | Fe2+ | ||||
�� | Ϊ����ʵ�����ο� | 298 | 3 | 6.0 | 0.30 |
�� | ̽���¶ȶԽ��ⷴӦ���ʵ�Ӱ�� | _________ | ______ | _______ | _________ |
�� | __________________ | <>298 | 10 | 6.0 | 0.30 |
��5�����������ͼʵ�������ߣ����㽵�ⷴӦ��50��150s�ڵķ�Ӧ���ʣ�v(p-CP)=_____________
��6��ʵ��ʱ���ڲ�ͬʱ��ӷ�Ӧ����ȡ������ʹ��ȡ��Ʒ�еķ�Ӧ����ֹͣ����������ʵ����������һ��Ѹ��ֹͣ��Ӧ�ķ�����__________________________��