题目内容
16.过氧化钠几乎与所有的常见非金属氧化物反应,如:2Na2O2+2CO2=2Na2CO3+O2 Na2O2+CO=Na2CO3
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式2Na2O2+2SO2═2Na2SO4,2Na2O2+2SO3═2Na2SO4+O2.
(2)通过比较可知,当非金属元素处于最高价态时,其氧化物与过氧化钠反应有氧气生成.
分析 由题给信息可知,过氧化钠与低价态的非金属氧化物发生化合反应,生成该非金属的最高价态的含氧酸盐,此时没有氧气产生;当非金属氧化物有高低价态时,过氧化钠与最高价态的非金属氧化物反应生成该非金属的最高价态的含氧酸盐和氧气,以此解答该题.
解答 解:(1)根据根据过氧化钠和二氧化碳的反应,可以推知过氧化钠和二氧化硫反应生成亚硫酸钠和氧气,亚硫酸钠易被氧气氧化为硫酸钠,即SO2+Na2O2=Na2SO4,三氧化硫和过氧化钠反应生成硫酸钠和氧气,即2Na2O2+2SO3═2Na2SO4+O2,
故答案为:2Na2O2+2SO2═2Na2SO4;2Na2O2+2SO3═2Na2SO4+O2;
(2)根据反应2Na2O+2CO2═2Na2CO3+O2,Na2O2+CO═Na2CO3和2Na2O2+2SO2═2Na2SO4,2Na2O2+2SO3═2Na2SO4+O2,比较可知:在氧化物中,当非金属元素处于最高价时,其氧化物与过氧化钠反应就有O2生成,故答案为:最高.
点评 本题考查过氧化钠知识,侧重于学生的分析能力和自学能力的考查,注意把握题给信息,具有分析和解决问题的能力,难度不大.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
6.A(g)+B(g)=C(g)△H=-Q1KJ/mol
D(g)+B(g)=E(g)△H=-Q2KJ/mol,
且Q1大于Q2,若A和D的混合气体1mol完全与B反应放出的热量为Q3KJ,则A与D的物质的量之比为( )
D(g)+B(g)=E(g)△H=-Q2KJ/mol,
且Q1大于Q2,若A和D的混合气体1mol完全与B反应放出的热量为Q3KJ,则A与D的物质的量之比为( )
| A. | (Q2-Q1):(Q1-Q3) | B. | (Q3-Q2):(Q1-Q3) | C. | (Q3-Q2):(Q3-Q1) | D. | (Q1-Q2):(Q3-Q1) |
1.生活中处处存在化学,下列说法不正确的是( )
| A. | 聚乳酸可用作手术缝合纱线、缓释药物材料 | |
| B. | 含钙、钡、铂等金属元素的物质有绚丽的颜色,可用于制造焰火 | |
| C. | 福尔马林用于标本的制作是利用了使蛋白质变性的性质 | |
| D. | 在清理厕所时洁厕灵和84消毒液不能混用,否则可能发生中毒现象 |
5.下列说法不正确的是( )
| A. | 均三甲苯在核磁共振氢谱中能出现两组峰,且其峰面积之比为3:1 | |
| B. | 按系统命名法,化合物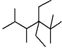 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 | |
| C. | 乙醇和二甲醚互为同分异构体,利用红外光谱法或核磁共振氢谱法均可鉴别两者 | |
| D. | 肌醇 与葡萄糖 与葡萄糖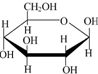 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 |
6.下列有关硅和硅的化合物的叙述中正确的是( )
| A. | 二氧化硅是良好的半导体材料,可用于制造集成电路、晶体管器件和硅芯片等 | |
| B. | 硅的化学性质很稳定,常温下与酸、碱、盐等难以反应 | |
| C. | 硅酸俗称水玻璃,是制备硅胶和木材防火剂的原料 | |
| D. | 向含有少量酚酞的硅酸钠溶液中逐滴加入稀盐酸,边加边振荡,可以看到溶液红色逐渐消失 |