题目内容
8.已知在绝热、容积固定的密闭容器中投入一定量的A、B.发生可逆反应:aA+bB?cC+d D,现有以下几种情况:①amolA分解的同时有cmolC生成
②bv(A)正=a v(B)正
③cv(B)正=bv(C)逆
④A、B、C、D的物质的量之比为a:b:c:d
⑤B的物质的量浓度保持不变
⑥气体的密度保持不变
⑦混和气体的平均摩尔质量保持不变
⑧容器内的温度保持不变
⑨混合气体的压强保持不变
若A、B、C、D均为气体,且a+b≠c+d,则能判断以上反应达到平衡状态的是③⑤⑦⑧⑨(填序号)
分析 可逆反应中正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、物质的量百分含量以及由此引起的一系列物理量不变时,该反应就达到平衡状态,据此分析解答.
解答 解:若A、B、C、D均为气体,且a+b≠c+d,
①无论该反应是否达到平衡状态,一定存在amolA分解的同时有cmolC生成,所以不能据此判断平衡状态,故错误;
②无论该反应是否达到平衡状态,一定存在bv(A)正=a v(B)正,所以不能据此判断平衡状态,故错误;
③可逆反应达到平衡状态时一定存在cv(B)正=bv(C)逆,所以能判断平衡状态,故正确;
④A、B、C、D的物质的量之比为a:b:c:d时该反应不一定达到平衡状态,与反应物的初始物质的量及转化率有关,故错误;
⑤B是气体,B的物质的量浓度保持不变,该反应达到平衡状态,故正确;
⑥如果这四种物质都是气体,则容器中密度始终不变,所以不能根据密度判断平衡状态,故错误;
⑦如果四种物质都是气体且a+b≠c+d,则反应前后混合气体平均摩尔质量改变,当混和气体的平均摩尔质量保持不变时,该反应达到平衡状态,故正确;
⑧该反应前后温度发生改变,当容器内的温度保持不变,该反应达到平衡状态,故正确;
⑨反应前后气体总物质的量改变,则压强改变,当混合气体的压强保持不变,该反应达到平衡状态,故正确;
所以能判断以上反应达到平衡状态的是③⑤⑦⑧⑨,
故答案为:③⑤⑦⑧⑨.
点评 本题考查化学平衡状态的判断,为高频考点,只有反应前后改变的物理量才能作为化学平衡状态判断依据,否则不能作为平衡状态判断依据,为易错题.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
18.下列除杂质的操作中不正确的是( )
| A. | Fe2O3中混有少量的Al2O3:加入过量烧碱溶液充分反应后过滤 | |
| B. | FeCl2溶液中混有FeCl3:加入过量铁粉充分反应后过滤 | |
| C. | Na2CO3固体中混有少量NaHCO3:加入适量NaOH溶液 | |
| D. | SiO2固体中混有少量的铁粉:用磁铁将铁粉吸出 |
13.在同温同压下,A容器中盛有H2,B容器中盛有NH3,若使它们所含的原子总数相等,则两种气体的物质的量之比( )
| A. | 2:1 | B. | 1:2 | C. | 2:3 | D. | 1:3 |
20.下列实验及操作方法正确的是( )
| A. | 配制一定物质的量浓度的溶液时,若摇匀后发现液面低于刻度线,要再用胶头滴管加水至刻度线 | |
| B. | 除去FeCl2溶液中的少量FeBr2,可先加入适量氯水,再用CCl4萃取分液 | |
| C. | 为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用 | |
| D. | 向溶液中先加入KSCN溶液无明显现象,再加入新制氯水,溶液呈红色,证明原溶液中含有Fe2+ |
 .
.
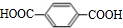 +nHOCH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$
+nHOCH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$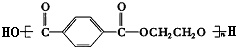 +(2n-1)H2O 其反应类型是:缩聚反应.
+(2n-1)H2O 其反应类型是:缩聚反应.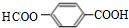 、
、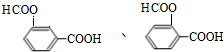 (其中两种).
(其中两种).