题目内容
1.阿伏伽德罗常数是物理学和化学中的一个重要常量.下列说法正确的是(NA为阿伏伽德罗常数)( )| A. | 28g氮气含有的原子数为NA | |
| B. | 4g金属钙的物质的量为1mol | |
| C. | 1mol O2分子的质量等于1mol氧原子的质量 | |
| D. | 24g O2分子和24g O3分子所含的氧原子数相等 |
分析 A.依据n=$\frac{m}{M}$计算物质的量结合氮气是双原子分子计算原子数;
B.依据n=$\frac{m}{M}$计算;
C.依据m=Mn计算,用微粒的摩尔质量和物质的量计算结果分析比较;
D.依据氧元素守恒结合n=$\frac{m}{M}$计算氧原子物质的量.
解答 解:A.28g氮气物质的量=$\frac{28g}{28g/mol}$=1mol,含有的原子数为2NA,故A错误;
B.4g金属钙的物质的量=$\frac{4g}{40g/mol}$=0.1mol,故B错误;
C.1molO2分子的质量为32g,1mol氧原子的质量为16g,两者质量不同,故C错误;
D.24gO2分子中 氧原子物质的量=$\frac{24g}{16g/mol}$=1.5mol,24gO3分子所含的氧原子物质的量=$\frac{24g}{16g/mol}$=1.5mol,所含氧原子数目相等,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的应用,主要是质量换算物质的量计算微粒数,熟悉相关公式是解题关键,题目难度不大.

练习册系列答案
相关题目
11.如图表示中和滴定前某同学的一个操作,下列叙述正确的是( )
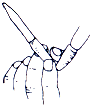

| A. | 这是一个错误操作 | |
| B. | 该操作是为了排除滴定管内气泡 | |
| C. | 该滴定管为酸式滴定管 | |
| D. | 该操作是为了调节滴定管内液体的液面高低 |
16.选用一种试剂能把物质的量浓度均为1mol/L的Na2SO4、Na2SO3、Na2S、Na2CO3和BaCl2五种无色溶液加以区别,这种试剂是( )
| A. | CaCl2 | B. | Ba(OH)2 | C. | H2SO4 | D. | HCl |
6.取100mL0.3mol•L-1的H2SO4溶液和300mL0.25mol•L-1的H2SO4溶液配成500mL的溶液所得溶液中H+的物质的量浓度为( )
| A. | 0.265mol•L-1 | B. | 0.525mol•L-1 | C. | 0.21mol•L-1 | D. | 0.42mol•L-1 |
3.A、B、D、E、F、G为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍.B 在D中充分燃烧能生成其最高价化合物BD2.E+与D2-具有相同的电子数.A在F中燃烧,产物溶于水得到一种强酸.G与D最外层电子数相等.回答下列问题:
(1)A在周期表中的位置是第一周期第ⅠA族
(2)D、E、G三种元素均可形成简单离子,其半径由大到小的顺序为r(S2-)>r(O2-)>r(Na+)(用离子符号表示)
(3)B、F、G三种元素形成的最高价氧化物对应的水化物中酸性最强的物质是高氯酸(填物质名称); B、D、G三种元素形成的最简单气态氢化物中的沸点最高的物质是H2O(填化学式)
(4)A与B形成的所有化合物中,等质量时耗氧量最大的物质的分子构型为正四面体形
(5)由这些元素组成的物质,其组成和结构信息如下表:
①a的电子式为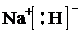 ;
;
②78g b中含有阴离子的物质的量为1mol;
③c的电子式为 ;
;
④单质B与d的浓溶液反应的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
(1)A在周期表中的位置是第一周期第ⅠA族
(2)D、E、G三种元素均可形成简单离子,其半径由大到小的顺序为r(S2-)>r(O2-)>r(Na+)(用离子符号表示)
(3)B、F、G三种元素形成的最高价氧化物对应的水化物中酸性最强的物质是高氯酸(填物质名称); B、D、G三种元素形成的最简单气态氢化物中的沸点最高的物质是H2O(填化学式)
(4)A与B形成的所有化合物中,等质量时耗氧量最大的物质的分子构型为正四面体形
(5)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 仅由A和E两元素组成的离子化合物 |
| b | 由D和E组成的离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 化学组成为A2GD4 |
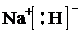 ;
;②78g b中含有阴离子的物质的量为1mol;
③c的电子式为
 ;
;④单质B与d的浓溶液反应的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
1.下列变化过程中,需吸收能量的是( )
| A. | 氢氧化钠与盐酸的反应 | B. | H+Cl→HCl | ||
| C. | 氯化铵与氢氧化钡晶体反应 | D. | 金属钠与水反应 |
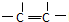
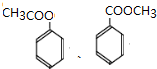 .
.