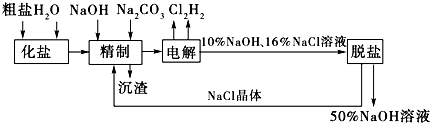
题目内容
3.A、B、D、E、F、G为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍.B 在D中充分燃烧能生成其最高价化合物BD2.E+与D2-具有相同的电子数.A在F中燃烧,产物溶于水得到一种强酸.G与D最外层电子数相等.回答下列问题:(1)A在周期表中的位置是第一周期第ⅠA族
(2)D、E、G三种元素均可形成简单离子,其半径由大到小的顺序为r(S2-)>r(O2-)>r(Na+)(用离子符号表示)
(3)B、F、G三种元素形成的最高价氧化物对应的水化物中酸性最强的物质是高氯酸(填物质名称); B、D、G三种元素形成的最简单气态氢化物中的沸点最高的物质是H2O(填化学式)
(4)A与B形成的所有化合物中,等质量时耗氧量最大的物质的分子构型为正四面体形
(5)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 仅由A和E两元素组成的离子化合物 |
| b | 由D和E组成的离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 化学组成为A2GD4 |
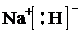 ;
;②78g b中含有阴离子的物质的量为1mol;
③c的电子式为
 ;
;④单质B与d的浓溶液反应的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
分析 A、B、D、E、F、G为短周期元素,非金属元素A最外层电子数与其周期数相同,则A为H元素;E+与D2-具有相同的电子数,则E处于IA族,D处于ⅥA族,则E为Na、D为O元素;B在D中充分燃烧生成其最高价化合物BD2,B的最高正化合价为+4,B的最外层电子数是其所在周期数的2倍,则B处于第二周期,故B为碳元素;A在F中燃烧,产物溶于水得到种强酸,则F为Cl,G与D最外层电子数相等,所以G是硫,由此分析解答.
解答 解:(1)A是氢,在周期表中的位置是第一周期第ⅠA族,故答案为:第一周期第ⅠA族;
(2)电子层数越多半径越大,电子层数相同时,核电荷数越多半径越小,所以离子半径大小为:r(S2-)>r(O2-)>r(Na+),故答案为:r(S2-)>r(O2-)>r(Na+);
(3)碳、氯、硫三种元素中,最高价氧化物对应的水化物中酸性最强的物质是高氯酸,碳、氧、硫三种元素氢化物中水与水分子间存在氢键,沸点异常的高,故答案为:高氯酸;H2O;
(4)氢与碳形成的所有烃中,等质量时耗氧量最大,也就是含氢量最高的甲烷,甲烷的分子构型为正四面体形,故答案为:正四面体形;
(5)①a仅由氢和钠两元素组成的离子化合物是氢化钠,电子式为: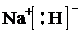 ,故答案为:
,故答案为: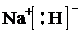 ;
;
②b由氧和钠组成的离子化合物,且原子数之比为1:1,是过氧化钠,78g过氧化钠的物质的量为1mol,含有阴离子过氧根离子的物质的量为1mol,故答案为:1;③③c化学组成为COCl2,其电子式为 ,故答案为:
,故答案为: ;
;
④单质碳与浓硫酸反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
点评 本题考查元素化合物推断,题目涉及的知识点较多,侧重于考查学生对所学知识点综合应用能力,题目难度中等.

| W | X | |
| Y | Z |
| A. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| B. | Z元素氧化物对应水化物的酸性一定强于Y | |
| C. | 简单阴离子还原性X大于Y | |
| D. | Z元素单质在化学反应中只表现氧化性 |
| A. | 通入X溶液浑浊,通入Y无明显现象 | B. | 通入X现象不明显,通入Y溶液浑浊 | ||
| C. | 通入X和Y溶液均无明显现象 | D. | 通入X和Y溶液均浑浊 |
| A. | 28g氮气含有的原子数为NA | |
| B. | 4g金属钙的物质的量为1mol | |
| C. | 1mol O2分子的质量等于1mol氧原子的质量 | |
| D. | 24g O2分子和24g O3分子所含的氧原子数相等 |
| A. | 若pH>7,则一定是c1V1≥c2V2 | |
| B. | 在任何情况下都是c(Na+)+c(H+)═c(CH3COO-)+c(OH-) | |
| C. | 当醋酸和氢氧化钠溶液恰好完全反应后,滴加酚酞溶液,颜色变红 | |
| D. | 反应的离子方程式为:H++OH-═H20 |
 下面如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )
下面如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )| A. | Penguinone的分子式为C10H12O | |
| B. | Penguinone的同分异构体中不可能有芳香醛 | |
| C. | Penguinone分子1mol能与3molBr2发生加成反应 | |
| D. | .Penguinone分子中所有碳原子可能处于同一平面上 |
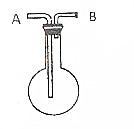 利用如图所示的装置收集以下7种气体(图中烧瓶位置不得移动)
利用如图所示的装置收集以下7种气体(图中烧瓶位置不得移动)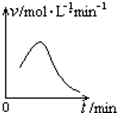 已知氯酸钾和亚硫酸氢钠发生氧化还原反应时,生成-1价的氯和+6价的硫的化合物,反应速率v和反应时间t的关系如图所示.
已知氯酸钾和亚硫酸氢钠发生氧化还原反应时,生成-1价的氯和+6价的硫的化合物,反应速率v和反应时间t的关系如图所示.