题目内容
3.(1)系统命名法命名: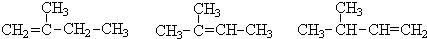
2-甲基-1-丁烯、2-甲基-2-丁烯、3-甲基-1-丁烯.
(2)有机物环癸五烯分子结构可表示为
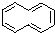 .试回答下列问题
.试回答下列问题①环癸五烯属于ab.
a.环烃 b.不饱和烃 c.饱和烃 d.芳香烃
②环癸五烯具有的性质bc.
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
③环癸五烯和足量的氢气反应后所得生成物的分子式为C10H20.
分析 (1)烯烃的命名选取含有碳碳双键的最长碳链为主链,距离碳碳双键最近的一端命名为1号碳;
(2)①只含有碳氢两种元素的化合物属于烃,含有环状结构的烃为环烃;
②该有机物含有碳碳双键,可发生加成、加聚和氧化反应;
③环癸五烯和足量的氢气反应得到环烷烃.
解答 解:(1)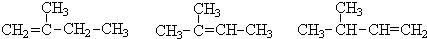 此三种烯烃含有碳碳双键的最长碳链均是4,故应为丁烯,双键分别在1、2号碳之间、2、3号碳之间和1、2号碳之间,分别在2号位、2号位和3号位上含有1个甲基,故分别命名为:2-甲基-1-丁烯、2-甲基-2-丁烯、3-甲基-1-丁烯,
此三种烯烃含有碳碳双键的最长碳链均是4,故应为丁烯,双键分别在1、2号碳之间、2、3号碳之间和1、2号碳之间,分别在2号位、2号位和3号位上含有1个甲基,故分别命名为:2-甲基-1-丁烯、2-甲基-2-丁烯、3-甲基-1-丁烯,
故答案为:2-甲基-1-丁烯;2-甲基-2-丁烯;3-甲基-1-丁烯;
(2)①环癸五烯分子结构可表示为: ,只含有碳氢两种元素的化合物属于烃,该有机物中含有双键,属于不饱和烃,含有环状结构的烃为环烃;故答案为:ab;
,只含有碳氢两种元素的化合物属于烃,该有机物中含有双键,属于不饱和烃,含有环状结构的烃为环烃;故答案为:ab;
②环癸五烯分子结构可表示为: ,该有机物含有碳碳双键,可发生加成反应、加聚反应和氧化反应,烃一般都难溶于水,碳原子数大于5常温下为液体;故答案为:bc;
,该有机物含有碳碳双键,可发生加成反应、加聚反应和氧化反应,烃一般都难溶于水,碳原子数大于5常温下为液体;故答案为:bc;
③环癸五烯的分子式为C10H10,环癸五烯和足量的氢气反应得到环烷烃C10H20,故答案为:C10H20.
点评 本题主要考查了烯烃的命名、有机物的结构和性质、同分异构体,明确有机物的结构与性质的关系即可解答,注意把握烯烃的性质来解答,题目难度中等.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
11.下列说法中,正确的是( )
| A. | CO2的摩尔质量为44g | |
| B. | 1molN2的质量是14g | |
| C. | 标准状况下,1molCO2所占的体积约是22.4L | |
| D. | 将40gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为1mol/L |
12.在下列溶液中,各组离子一定能够大量共存的是( )
| A. | 使酚酞溶液变红的溶液:Na+、Cl-、SO42-、Fe3+ | |
| B. | 含有大量Al3+的溶液中:Na+、NH4+、SO42-、Cl- | |
| C. | 含有大量Fe3+的溶液中:Na+、Mg2+、NO3-、SCN- | |
| D. | 碳酸氢钠溶液:K+、SO42-、Cl-、H+ |
16.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 透明溶液中:K+、Cu2+、SO42-、Cl- | |
| B. | KI水溶液中:K+、NO3-、SO42-、H+ | |
| C. | 使紫色石蕊试液变蓝色的溶液:K+、Na+、HS-、Cl- | |
| D. | 水电离出的c(H+)=1×10-14mol•L-1的溶液:K+、NH4+、AlO2-、Br- |
15.下列说法中,不正确的是( )
| A. | 反应热指的是反应过程中放出的热量 | |
| B. | 原电池的负极发生氧化反应 | |
| C. | 伴随能量变化的不一定是化学变化 | |
| D. | 电解池的阳极发生氧化反应 |
12.黄铁矿(主要成分FeS2)、黄铜矿(主要成分CuFeS2)均是自然界中的常见矿物资源.
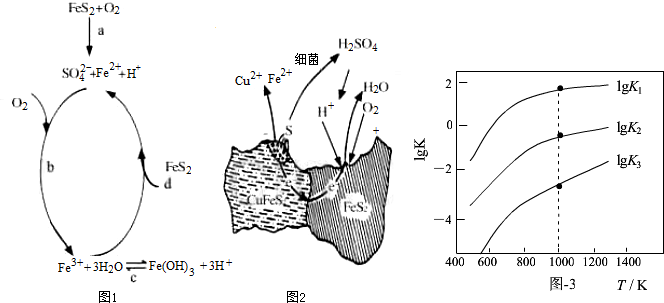
(1)Stumm和Morgan提出黄铁矿在空气中氧化的四步反应如题图1所示:
①a反应中每生成1molFeSO4转移电子的物质的量为7mol.
②d反应的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+.
(2)用细菌冶铜时,当黄铜矿中伴有黄铁矿可明显提高浸取速率,其原理如题图2
①冶炼过程中,正极周围溶液的pH增大(选填:“增大”、“减小”或“不变”)
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见下表),其相关反应的平衡常数的对数值与温度的关系如题图3.
①上述反应中,△H1>0(选填:“>”或“<”).
②提高硫的脱除率可采取的措施有升高温度(举1例).
③1000K时,平衡常数的对数lgK1、lgK2和lgK3之间的关系为lgK2=lgK1+lgK3.
(1)Stumm和Morgan提出黄铁矿在空气中氧化的四步反应如题图1所示:
①a反应中每生成1molFeSO4转移电子的物质的量为7mol.
②d反应的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+.
(2)用细菌冶铜时,当黄铜矿中伴有黄铁矿可明显提高浸取速率,其原理如题图2

①冶炼过程中,正极周围溶液的pH增大(选填:“增大”、“减小”或“不变”)
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见下表),其相关反应的平衡常数的对数值与温度的关系如题图3.
| 相关反应 | 反应热 | 平衡常数K |
| FeS2(s)+H2(g)?FeS(s)+H2S(g) | △H1 | K1 |
| $\frac{1}{2}$FeS2(s)+H2(g)?$\frac{1}{2}$Fe(s)+H2S(g) | △H2 | K2 |
| FeS(s)+H2(g)?Fe(s)+H2S(g) | △H3 | K3 |
②提高硫的脱除率可采取的措施有升高温度(举1例).
③1000K时,平衡常数的对数lgK1、lgK2和lgK3之间的关系为lgK2=lgK1+lgK3.
13.简单原子的原子结构可用下图形象的表示:
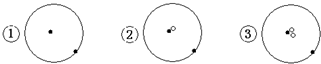
其中 表示质子或电子,
表示质子或电子, 表示中子,则下列有关的叙述正确的是( )
表示中子,则下列有关的叙述正确的是( )

其中
 表示质子或电子,
表示质子或电子, 表示中子,则下列有关的叙述正确的是( )
表示中子,则下列有关的叙述正确的是( )| A. | ①②③是三种化学性质不同的粒子 | B. | ①②③具有相同的质量数 | ||
| C. | ①②③为同素异形体 | D. | ①②③互为同位素 |
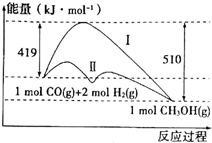 工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g),反应过程中的能量变化情况如图所示.
工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g),反应过程中的能量变化情况如图所示. 按如图所示装置进行实验,并回答下列问题:
按如图所示装置进行实验,并回答下列问题: