题目内容
9.在标准状况下进行下列实验:甲、乙、丙各取30.00ml同浓度的盐酸,加入同一镁铝合金,产生气体,测得有关数据列表如表:| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量 | 0.255g | 0.385g | 0.459g |
| 气体体积 | 280mL | 336mL | 336mL |
①盐酸的物质的量浓度为1 mol•L-1.
②据甲(填实验序号)中的数据,可计算出合金中镁与铝的物质的量分别为0.005mol;0.005mol.
(2)在丙实验之后,向容器中加入一定量1.00mol•L-1的NaOH溶液,使合金中的铝恰好完全溶解,再滤出不溶固体.请计算:
①滤液中的溶质及其物质的量是NaCl为0.03mol,NaAlO2为0.009mol.
②加入NaOH溶液的体积为39mL.
分析 (1)乙、丙中盐酸完全,可以根据反应生成氢气体积计算盐酸的物质的量浓度,根据n=$\frac{V}{Vm}$计算氢气的物质的量,根据氢元素守恒可知n(HCl)=2n(H2),据此计算;
(2)甲中盐酸有剩余,金属完全反应,此时生成氢气280mL,故可以根据甲组数据计算金属的物质的量之比,令镁、铝的物质的量分别为xmol、ymol,根据二者质量之和与电子转移守恒列方程计算x、y的值,据此解答;
(3)①在丙实验之后,向容器中加入一定量1.00mol/L的NaOH溶液,使合金中的铝恰好完全溶解,再滤出不溶固体,溶液中溶质为NaCl、NaAlO2,根据氢气的体积计算HCl的物质的量,溶液中(NaCl)=n(Cl-),设0.459g合金中含铝的物质的量为xmol,结合(1)中Mg、Al物质的量关系,根据质量列方程计算,由Al元素守恒n(NaAlO2)=n(Al);
②根据钠离子守恒n(NaOH)=n(NaCl)+n(NaAlO2),进而计算氢氧化钠的体积.
解答 解(1)乙、丙中盐酸完全,可以根据反应生成氢气体积计算盐酸的物质的量浓度,盐酸完全反应生成氢气336mL,氢气的物质的量为$\frac{0.336L}{22.4L/mol}$=0.015mol,根据氢元素守恒可知n(HCl)=2n(H2)=2×0.015mol=0.03mol,故盐酸的物质的量浓度为$\frac{0.03mol}{0.03L}$=1mol/L,
故答案为:1;
(3)甲中盐酸有剩余,金属完全反应,此时生成氢气280mL,故可以根据甲组数据计算金属的物质的量之比,令镁、铝的物质的量分别为xmol、ymol,根据二者质量可知24x+27y=0.255,根据电子转移守恒有2x+3y=$\frac{0.28L}{22.4L/mol}$×2,联立方程解得:x=0.005、y=0.005,故合金中镁与铝的物质的量分别为0.005mol、0.005mol,故答案为:甲;0.005mol;0.005mol;
(3)①在丙实验之后,向容器中加入一定量1.00mol/L的NaOH溶液,使合金中的铝恰好完全溶解,再滤出不溶固体,溶液中溶质为NaCl、NaAlO2,
盐酸完全反应生成氢气336mL,氢气的物质的量=0.336L÷22.4L/mol=0.015mol,根据氢元素守恒可知n(HCl)=2n(H2)=2×0.015mol=0.03mol,溶液中(NaCl)=n(Cl-)=0.03mol,
设0.459g合金中含铝的物质的量为xmol,由(1)中计算可知,Mg的物质的量也是x mol,则:27x+24x=0.459,解得x=0.009mol,n(NaAlO2)=n(Al)=0.009mol,
故答案为:NaCl为0.03mol,NaAlO2为0.009mol.
②根据钠离子守恒n(NaOH)=n(NaCl)+n(NaAlO2)=0.03mol+0.009mol=0.039mol,故需要氢氧化钠溶液的体积=0.039mol÷1mol/L=0.039L=39mL,
故答案为:39mL.
点评 本题考查混合物的计算,根据表中数据关系判断反应的过量问题是关键,侧重考查学生对数据分析处理能力,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | Si可用于制造太阳能电池 | |
| B. | Na2O2可用于呼吸面具中作为氧气的来源 | |
| C. | Fe2O3常用于制造红色油漆和涂料 | |
| D. | 常温下可用铝制容器盛装稀硫酸 |
探究一
(1)将粗铁粒投入某浓度硝酸中,某同学观察该实验现象时发现,反应进行一段时间后,反应开始逐渐加快.请分析反应逐渐加快的可能原因反应放热,一段时间后溶液温度升高,反应速率加快;②由于铁中含杂质铜,反应时形成Fe-Cu微型原电池,加快反应速率.
(2)另称取粗铁粒10g放入某浓度硝酸中,充分反应后得到溶液X并收集到气体Y.为了探究溶液X中铁元素的价态,同学甲设计如下实验:有药品和仪器:0.1mol•L-1 KSCN溶液;0.1mol•L-1 KI溶液;0.2mol•L-1酸性高锰酸钾溶液;氯水等;试管和滴管.
请你设计简单实验,探究上述猜想是否正确,填写下列实验报告:
| 实验步骤 | 现象 | 结论 | 离子方程式 |
| 第一步 | 取2-3mL溶液装于试管,向试管中加入几滴KSCN溶液. | 若溶液变红色,则溶液含有Fe3+; 若无现象,则不含Fe3+ | Fe3++3SCN-=Fe(SCN)3 |
| 第二步 | 另取少量溶液装于试管,向试管里滴加几滴酸性高锰酸钾溶液 | 若溶液紫色褪去,则溶液含有Fe2+; 若无明显变化,则不含Fe3+. | 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O |
为了探究气体Y的成分,同学乙设计了如下装置(不考虑NO2转化为N2O4)
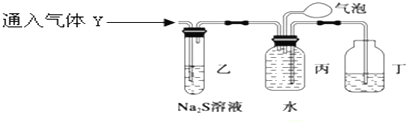
(3)装置乙的作用:验证NO2的存在并除去NO2.
(4)装置丙收集到满气体后,通过气泡鼓入空气后,有红棕色气体生成,能否确定气体Y中含NO?说明理
由.不能确定,由于NO2与水反应也能生成NO,故不能确定气体Y中含NO.
(5)同学丁为了探究气体Y的组成,将224mL气体Y通入足量的NaOH溶液中,气体被完全吸收,所得溶液再用0.15mol/L-1酸性KMnO4溶液滴定,消耗20mL KMnO4溶液.则气体Y中NO、NO2的体积比为1:3.(已知2NO2+2NaOH=NaNO3+NaNO2+H2O和NO2+NO+2NaOH=2NaNO2+H2O)
| A. | K1=16 | B. | K1=8 | C. | K2=1 | D. | K2=0.5 |
| A. |  → → | |
| B. | CH2═CH-CH2-CH3+HCl$→_{△}^{催化剂}$ | |
| C. | CH3-CH═CH2+H2O$→_{加热、加压}^{催化剂}$ | |
| D. | nCH2═CH2+nCH2═CH-CH3$→_{△}^{催化剂}$ |
| A. | 1g酒精和1g水混合后的总质量 | |
| B. | 100mL酒精与100mL水混合均匀后所得溶液的总体积 | |
| C. | 温度一定时1gH2O溶解1g硝酸钾后,所得溶液的质量 | |
| D. | 1g氢氧化钠溶液和1g醋酸溶液混合后溶液的质量 |
| A. | 含1 mol FeCl3的饱和溶液最多可形成胶体粒子数为NA | |
| B. | 4.6 g Na与稀盐酸反应,转移电子数一定为0.2NA | |
| C. | 10.6 g Na2C03晶体中含CO${\;}_{3}^{2-}$数目为0.1NA | |
| D. | 常温下,22g CO2含碳氧双键数目为NA |