题目内容
【题目】羟胺的电离方程式为:NH2OH+H2O![]() NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL0.lmol/L胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法错误的是( )
NH3OH++OH-(25℃时,Kb=9.0×10-9)。用0.lmol/L盐酸滴定20mL0.lmol/L胺溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法错误的是( )
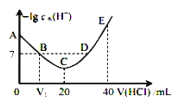
A.图中V1<10
B.A点对应溶液的pH=9.5
C.A、B、C、D四点中酸性最强的点为C点
D.E点对应溶液中存在:c(H+)=c(OH-)+c(NH3OH+)+2c(NH2OH)
【答案】C
【解析】
A.羟胺是一元弱碱,若V1=10,则反应恰好起始时产生等量的NH2OH和NH3OH+,由Kb=9.0×10-9得到![]() 即NH3OH+的水解比NH2OH电离程度大,溶液呈酸性,而A点时水的电离达到107 molL1,说明NH3OH+的水解程度和NH2OH抑制水的程度相当,因此NH3OH+物质的量浓度要小于NH2OH物质的量浓度,故滴加的HCl小于10mL,所以V1应<10,故A正确;
即NH3OH+的水解比NH2OH电离程度大,溶液呈酸性,而A点时水的电离达到107 molL1,说明NH3OH+的水解程度和NH2OH抑制水的程度相当,因此NH3OH+物质的量浓度要小于NH2OH物质的量浓度,故滴加的HCl小于10mL,所以V1应<10,故A正确;
B.羟胺的电离方程式为:NH2OH+H2O![]() NH3OH++OH,已知25℃时,其电离平衡常数为Kb=9.0×109,
NH3OH++OH,已知25℃时,其电离平衡常数为Kb=9.0×109,![]() ,
,![]() ,pOH = 4.5,pH = 144.5 =9.5,故B正确;
,pOH = 4.5,pH = 144.5 =9.5,故B正确;
C.A点是NH2OH ,溶液显碱性,B点溶液产生NH3OH+水解,水解程度等于NH2OH的电离程度,溶液呈中性,C点只有一种溶质,NH3OH+水解显酸性,D点溶液HCl过量,溶液呈酸性,因此酸性最强的是D电,故C错误;
D.E点时加入HCl的体积为40mL,根据电荷守恒:c(H+)+c(NH3OH+)=c(OH)+c(Cl),根据物料守恒:2c(NH3OH+)+2c(NH2OH)=c(Cl),则有c(H+)=c(OH)+c(NH3OH+)+2c(NH2OH),故D正确。
综上所述,答案为C。

【题目】FeSO4溶液放置在空气中容易变质,因此为了方便使用Fe2+,实验室中常保存硫酸亚铁铵晶体[俗称“摩尔盐”,化学式为(NH4)2Fe(SO4)26H2O],它比绿矾或绿矾溶液更稳定。
I.某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都经过煮沸、冷却后再使用。向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作_______、冷却结晶、过滤、洗涤和干燥后得到一种浅蓝绿色的晶体。
II.实验探究影响溶液中Fe2+稳定性的因素
(1)配制0.8 mol/L的FeSO4溶液(pH=4.5)和0.8 mol/L的(NH4)2Fe(SO4)2溶液(pH=4.0),各取2 mL上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加2滴0.01mol/L的KSCN溶液,15min后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液,FeSO4溶液则出现淡黄色浑浊。
(资料1)
沉淀 | Fe(OH)2 | Fe(OH)3 |
开始沉淀 pH | 7.6 | 2.7 |
完全沉淀 pH | 9.6 | 3.7 |
①请用离子方程式解释FeSO4溶液产生淡黄色浑浊的原因___________________。
②讨论影响Fe2+稳定性的因素,小组同学提出以下3种假设:
假设1:其他条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中Fe2+稳定性较好。
假设2:其他条件相同时,在一定 pH范围内,溶液 pH越小Fe2+稳定性越好。
假设3:__________________________________________________。
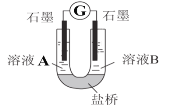
(2)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分别控制溶液A(0.2 mol/L NaCl)和溶液B(0.1mol/L FeSO4)为不同的 pH,观察记录电流计读数,对假设2进行实验研究,实验结果如下表所示。
序号 | A 0.2mol/LNaCl | B 0.1mol/LFeSO4 | 电流计读数 |
实验1 | pH=1 | pH=5 | 8.4 |
实验2 | pH=1 | pH=1 | 6.5 |
实验3 | pH=6 | pH=5 | 7.8 |
实验4 | pH=6 | pH=1 | 5.5 |
(资料2)原电池装置中,其他条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原电池的电流越大。
(资料3)常温下,0.1mol/LpH=1的FeSO4溶液比pH=5的FeSO4溶液稳定性更好。
根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U型管中左池的电极反应式_________________。
②对比实验1和2(或3和4),在一定pH范围内,可得出的结论为______ 。
③对比实验_____和_____ 还可得出在一定 pH范围内,溶液酸碱性变化是对O2氧化性强弱的影响因素。
④对(资料3)实验事实的解释为____________________。