题目内容
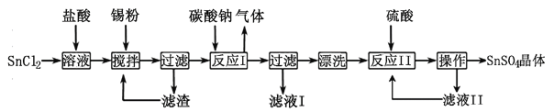
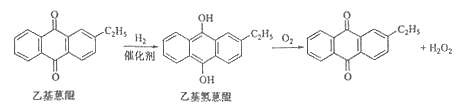
【题目】化学——选修2:化学与技术]双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:
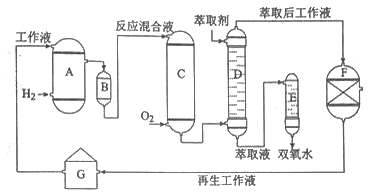
A.氢化釜 |
B.过滤器 |
C.氧化塔 |
D.萃取塔 |
E.净化塔
F.工作液再生装置
G.工作液配制装置 生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是 ,循环使用的原料是 ,配制工作液时采用有机溶剂而不采用水的原因是 。
(2)氢化釜A中反应的化学方程式为 ,进入氧化塔C的反应混合液中的主要溶质为 。
(3)萃取塔D中的萃取剂是,选择其作萃取剂的原因是 。
(4)工作液再生装置F中要除净残留的H2O2,原因是 。
(5)双氧水浓度可在酸性条件下用 KMnO4溶液测定,该反应的离子方程式为___________一种双氧水的质量分数为27.5%,(密度为1.10g·cm3),其浓度为 mol/L。
【答案】(1)氢气和氧气,乙基蒽醌,乙基蒽醌不溶于水,易溶于有机溶剂;
(2)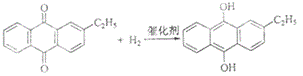 ,乙基氢蒽醌;
,乙基氢蒽醌;
(3)水,H2O2溶于水被水萃取,乙基蒽醌不溶于水;
(4)H2O2分解放出氧气,与氢气混合,易发生爆炸;
(5)5H2O2+6H++2MnO4-=2Mn2++8H2O+5O2↑,8.9mol·L-1。
【解析】试题分析:(1)根据反应原理,两式相加,乙基蒽醌作催化剂,使H2+O2=H2O2,因此理论上消耗的原料是氢气和氧气,循环使用原料是乙基蒽醌,根据题意,乙基蒽醌不溶于水,易溶于有机溶剂;(2)氢化釜A,发生的反应是乙基蒽醌和氢气的反应,因此反应方程式为: ,氧化塔C中发生反应是乙基氢蒽醌和氧气的反应,因此混合液中的主要溶质为乙基氢蒽醌;(3)过氧化氢易溶于水,乙基蒽醌不溶于水,因此用水进行萃取;(4)过氧化氢不稳定,易分解成氧气,氢气与氧气混合易发生爆炸;(5)H2O2既有氧化性又有还原性,高锰酸钾溶液的氧化性把H2O2氧化成氧气,根据化合价配平法进行配平,因此反应方程式为:H2O2+6H++2MnO4-=2Mn2++8H2O+5O2↑,根据c=1000ρw%/M,代入数值,得出c=8.9mol·L-1。
,氧化塔C中发生反应是乙基氢蒽醌和氧气的反应,因此混合液中的主要溶质为乙基氢蒽醌;(3)过氧化氢易溶于水,乙基蒽醌不溶于水,因此用水进行萃取;(4)过氧化氢不稳定,易分解成氧气,氢气与氧气混合易发生爆炸;(5)H2O2既有氧化性又有还原性,高锰酸钾溶液的氧化性把H2O2氧化成氧气,根据化合价配平法进行配平,因此反应方程式为:H2O2+6H++2MnO4-=2Mn2++8H2O+5O2↑,根据c=1000ρw%/M,代入数值,得出c=8.9mol·L-1。