题目内容
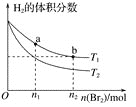
【题目】25℃时,氯水中部分含氯的物质的量浓度分数(某物质的物质的量浓度占各物质的量浓度之和的百分数)与pH的关系如图所示。下列叙述正确的是( )

A.pH=1的新制氯水中,c(Cl2)>c(ClO-)>c(HClO)
B.随着pH增大,溶液颜色不断加深
C.pH>10时,溶液中含氯微粒主要为ClO-和Cl-
D.pH=4的氯水中加入NaOH溶液,只发生离子反应HClO+OH-=ClO-+H2O
【答案】C
【解析】
A.根据pH=1时溶液中各种微粒的含量分步解答;
B.在氯水中只有Cl2是有色物质,其余物质均为无色,根据Cl2与溶液pH关系判断;
C.Cl2在水中存在化学平衡:Cl2+H2O![]() HCl+HClO,根据溶液的酸碱性及图示分析解答;
HCl+HClO,根据溶液的酸碱性及图示分析解答;
D.在pH=4的氯水中含有HCl、Cl2、HClO等,结合物质的化学性质分析。
A.根据图示可知,在pH=1时,氯水中各种微粒的含量:c(Cl2) >c(HClO)>c(ClO-),A错误;
B.在氯水中只有Cl2是有色物质,其余物质均为无色,由图示可知,随着溶液pH的增大,Cl2的含量逐渐降低,因此溶液的颜色逐渐变浅,B错误;
C.Cl2在水中存在化学平衡:Cl2+H2O![]() HCl+HClO,当溶液pH>10时,发生反应HCl+NaOH=NaCl+H2O,HClO+NaOH=NaClO+H2O,溶液中Cl2及HClO很少,根据图示也可看出溶液中含氯微粒主要为ClO-和Cl-,C正确;
HCl+HClO,当溶液pH>10时,发生反应HCl+NaOH=NaCl+H2O,HClO+NaOH=NaClO+H2O,溶液中Cl2及HClO很少,根据图示也可看出溶液中含氯微粒主要为ClO-和Cl-,C正确;
D.在pH=4的氯水中含有大量的HCl、Cl2、HClO等,所以发生的反应,有H++OH-=H2O、Cl2+2OH-=Cl-+ClO-+H2O,HClO+OH-=ClO-+H2O,所以不仅有HClO+OH-=ClO-+H2O,D错误;
故合理选项是C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目