题目内容
【题目】用![]() 代替
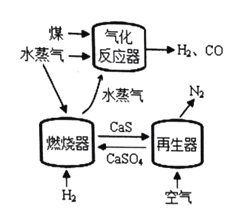
代替![]() 与燃料反应是一种高效、清洁、经济的新型燃烧技术,如图所示。
与燃料反应是一种高效、清洁、经济的新型燃烧技术,如图所示。
燃烧器中反应①![]() (主反应)
(主反应)
反应②![]() (副反应)
(副反应)
再生器中反应:![]()
(1)气化反应器中发生反应的化学方程式是 ______。
(2)燃烧器中![]() 物质的量分数随温度T、压强p
物质的量分数随温度T、压强p![]() 的变化曲线见图,从图中可以得出三条主要规律:
的变化曲线见图,从图中可以得出三条主要规律:
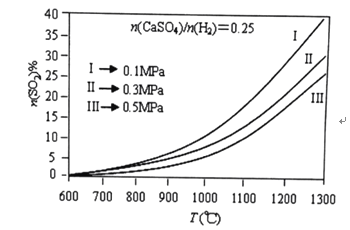
①其他条件不变,温度越高,![]() 含量越高;
含量越高;
②______ ;
③______ ;
由图可知,为减少![]() 的排放量,可采取的措施是 ______。
的排放量,可采取的措施是 ______。
(3)该燃烧技术中可循环的物质除![]() 、CaS外,还有 ______
、CaS外,还有 ______ ![]() 写名称
写名称![]() 。
。
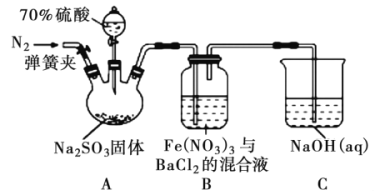
(4)欲采用氯化钯![]() 溶液除去
溶液除去![]() 中的CO,完成以下实验装置图:______
中的CO,完成以下实验装置图:______![]() 注:
注:![]() 。
。

(5)CO2在自然界循环时可与![]() 反应,
反应,![]() 是一种难溶物质,其
是一种难溶物质,其![]() 。现将
。现将![]()
![]() 的
的![]() 溶液与一定浓度的
溶液与一定浓度的![]() 溶液等体积混合生成沉淀,计算应加入
溶液等体积混合生成沉淀,计算应加入![]() 溶液的最小浓度为 ______(保留二位有效数字)。
溶液的最小浓度为 ______(保留二位有效数字)。
【答案】![]() 在温度一定时,压强越高,
在温度一定时,压强越高,![]() 含量越低 其它条件不变时,压强越小,温度对
含量越低 其它条件不变时,压强越小,温度对![]() 含量的影响越明显 降低温度,增加压强 水蒸气
含量的影响越明显 降低温度,增加压强 水蒸气 
![]()
【解析】
(1)根据图1的流程图可知,气化反应器中反应物为碳和水,生成物为氢气和一氧化碳,反应方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)根据图2可知,在温度一定时,压强越高,![]() 含量越低;其它条件不变时,压强越小,温度对
含量越低;其它条件不变时,压强越小,温度对![]() 含量的影响越明显;根据图2可知,温度越低,压强越大,
含量的影响越明显;根据图2可知,温度越低,压强越大,![]() 含量越小,所以要减少
含量越小,所以要减少![]() 的排放量,可以降低温度,增加压强,故答案为:在温度一定时,压强越高,
的排放量,可以降低温度,增加压强,故答案为:在温度一定时,压强越高,![]() 含量越低;其它条件不变时,压强越小,温度对
含量越低;其它条件不变时,压强越小,温度对![]() 含量的影响越明显;降低温度,增加压强;
含量的影响越明显;降低温度,增加压强;
(3)根据图1的流程图可知,该燃烧技术中可循环的物质除![]() 、CaS外,还有水蒸气,故答案为:水蒸气;
、CaS外,还有水蒸气,故答案为:水蒸气;
(4)欲采用氯化钯![]() 溶液除去
溶液除去![]() 中的CO,需要用一个洗气装置,装置中装足量的
中的CO,需要用一个洗气装置,装置中装足量的![]() 溶液,装置图为
溶液,装置图为 ,故答案为:
,故答案为: ;
;
(5)Na2CO3溶液的浓度为![]() ,等体积混合后溶液中
,等体积混合后溶液中![]() ,根据
,根据![]() 可知,
可知,![]() ,原溶液
,原溶液![]() 溶液的最小浓度为混合溶液中
溶液的最小浓度为混合溶液中![]() 的2倍,故原溶液
的2倍,故原溶液![]() 溶液的最小浓度为
溶液的最小浓度为![]() ,故答案为:
,故答案为:![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】NaHSO3可被过量KIO3氧化,当NaHSO3完全消耗时即有I2析出。某课题组用淀粉作指示剂,通过测定溶液变蓝所用时间来探究影响化学反应速率的因素。
(1)写出NaHSO3溶液与过量KIO3溶液反应生成I2的离子方程式:____________。
(2)调节反应物浓度和温度进行对比实验,记录结果如下:
编号 | 0.02mol/LNaHSO3溶液/mL | 0.02mol/LKIO3溶液/mL | H2O/mL | 反应温度/℃ | 溶液变蓝的时间t/s |
① | 10 | 15 | a | 10 | t1 |
② | 10 | 40 | 0 | 10 | t2 |
③ | 10 | b | 0 | 20 | t3 |
表中a=________,b=________。
(3)改变反应温度,重复实验③,得到温度(T)与溶液变蓝所需时间(t)的关系如下图所示(“×××”表示超过50℃后溶液不会再变蓝)。

①在30℃下,若溶液变蓝时,I2的物质的量为n mol,则从反应开始至溶液变蓝,IO3-的平均反应速率______mol·L-1·s-1(写出表达式即可,不要化简)。
②根据图像,请你分析温度低于50℃时,溶液变蓝所需时间与反应温度的关系:____。
(4)将NaHSO3溶液与KIO3溶液混合(预先加入可溶性淀粉为指示剂),用速率检测仪检测出起始阶段反应速率逐渐增大,一段时间后反应速率又逐渐减小。课题组对起始阶段反应速率逐渐增大的原因提出如下假设,请你完成假设二:
假设一:反应生成的I2对反应起催化作用;
假设二:_________________________________________;
(5)请你设计实验验证上述假设一,完成下表中内容(反应速率可用测速仪测定):____。
实验方案(不要求写出具体操作过程) | 预期实验现象和结论 |