题目内容
5.将5.08g由Na2CO3和NaHCO3组成的固体混合物完全溶于水,制成溶液,然后向该溶液中逐滴加入2mol•L-1的盐酸,所加人盐酸的体积与产生CO2体积(标准状况)的关系如图所示.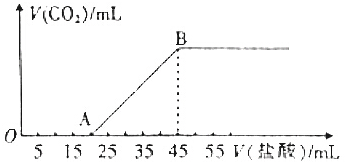
(1)写出OA段所发生反应的离子方程式:CO32-+H+═HCO3-.
(2)当加人35mL盐酸时,产生的CO2在标准状况下的体积为0.672L
(3)原混会物中Na2CO3和NaHCO3入的物质的量之比为4:1.
分析 (1)Na2CO3和NaHCO3组成的混合物中加入盐酸,先发生碳酸钠与盐酸反应生成碳酸氢钠与氯化钠,然后碳酸氢钠与盐酸反应生成二氧化碳气体;
(2)结合图象可知,当加入35mL盐酸时,20~35mL发生碳酸氢钠与盐酸的反应生成二氧化碳气体;
(3)根据OA段的反应及消耗盐酸的量计算出碳酸钠的物质的量,再根据总质量计算出碳酸氢钠的物质的量,最后计算出二者的物质的量之比.
解答 解:(1)加入盐酸后碳酸钠先与盐酸反应生成碳酸氢钠:Na2CO3+HCl═NaHCO3+NaCl,所以OA段的离子反应方程式为:CO32-+H+═HCO3-,
故答案为:CO32-+H+═HCO3-;
(2)结合图象可知,当加入35mL盐酸时,25~35mL发生碳酸氢钠与盐酸的反应生成二氧化碳气体,
设生成二氧化碳的物质的量为n,生成气体时消耗的酸的物质的量为(35-20)×10-3L×2mol•L-1=0.03mol,则
HCO3-+H+═CO2↑+H2O
1 1
0.03mol n
故n=0.03mol,标准状况下其体积为0.03mol×22.4L/mol=0.672L,
故答案为:0.672L;
(3)设碳酸钠、碳酸氢钠物质的量分别为x、y,则
根据OA段的反应Na2CO3+HCl═NaHCO3+NaCl可知碳酸钠的物质的量为:x=2mol/L×0.02L=0.04mol,
根据总质量可得:84g/mol•y+106g/mol×0.04mol=5.08g,解得:y=0.01mol,
故原混会物中Na2CO3和NaHCO3的物质的量之比为0.04mol:0.01mol=4:1,
故答案为:4:1.
点评 本题考查混合物反应的计算,题目难度中等,明确反应的先后顺序及图象中每段图象对应的化学反应是解答本题的关键,试题培养了学生的分析能力及化学计算能力.

| A. | 实验室保存溴时,常在保存液溴的试剂瓶中加入少量水来防止溴挥发 | |
| B. | 常将钠保存在煤油中 | |
| C. | 新制氯水应密封保存在棕色试剂瓶中 | |
| D. | 取碘水于试管中,加入CCl4,振荡后静置,溶液分层,上层呈紫红色 |
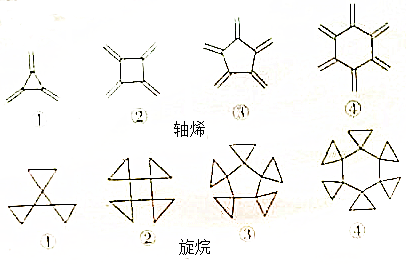
 ,Y
,Y .
.
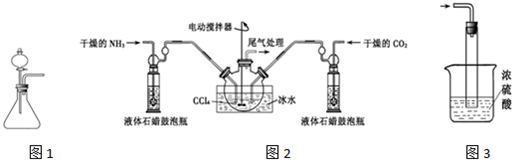
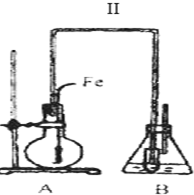 色沉淀,其作用是检验溴离子;装置(Ⅱ)还可起到的作用是防倒吸.
色沉淀,其作用是检验溴离子;装置(Ⅱ)还可起到的作用是防倒吸.