题目内容
【题目】某研究小组为了验证反应物浓度对反应速率的影响,选用硫酸酸化的高锰酸钾溶液与草酸H2C2O4溶液在室温下进行反应。实验中所用的草酸为稀溶液,视为强酸。
(1)写出硫酸酸化的高锰酸钾氧化稀草酸溶液的离子方程式__________。
(2)该小组进行了实验I,数据如下。
H2SO4溶液 | KMnO4溶液 | H2C2O4溶液 | 褪色时间(分:秒) |
1mL 2mol/L | 2mL 0.01mol/L | 1mL 0.1mol/L | 2:03 |
1mL 2mol/L | 2mL 0.01mol/L | 1mL 0.2mol/L | 2:16 |
一般来说,其他条件相同时,增大反应物浓度,反应速率___________(填“增大”或“减小”)。但分析该实验数据,得到的结论是在当前实验条件下,增大草酸浓度,反应速率减小。
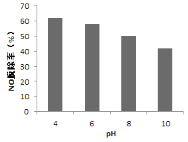
(3)该小组欲探究出现上述异常现象的原因,在实验I的基础上,只改变草酸溶液浓度进行了实验II,获得实验数据并绘制曲线图如下。

该小组查阅资料获取如下信息,其中能够解释MO变化趋势的是___________。
a | KMnO4与H2C2O4反应是分步进行的,反应过程中生成Mn(VI)、Mn(III)、Mn(IV),最终变为无色的Mn(II)。(括号中罗马数字表示锰的化合价) |
b | 草酸根易与不同价态锰离子形成较稳定的配位化合物。 |
c | 草酸稳定性较差,加热至185℃可分解。 |
(4)该小组为探究ON段曲线变化趋势的原因,又进行了实验III,所得数据如下。
H2SO4溶液 | Na2SO4固体 | KMnO4溶液 | H2C2O4溶液 | 褪色时间(分:秒) |
1mL 0.1mol/L | 1.9×10-3mol | 2mL 0.01mol/L | 1mL 0.2mol/L | 16:20 |
1mL 0.5mol/L | 1.5×10-3mol | 2mL 0.01mol/L | 1mL 0.2mol/L | 8:25 |
1mL 1.0mol/L | 1.0×10-3mol | 2mL 0.01mol/L | 1mL 0.2mol/L | 6:15 |
1mL 2.0mol/L | 0 | 2mL 0.01mol/L | 1mL 0.2mol/L | 2:16 |
该小组进行实验III的目的是____________________________________________。
(5)综合实验I、II、III,推测造成曲线MN变化趋势的原因________________。
a.当草酸浓度较小时,C2O42-起主要作用,草酸浓度越大,反应速率越小
b.当草酸浓度较小时,H+起主要作用,草酸浓度越大,反应速率越大
c.当草酸浓度较大时,C2O42-起主要作用,草酸浓度越大,反应速率越小
d.当草酸浓度较大时,H+起主要作用,草酸浓度越大,反应速率越大
【答案】2MnO4- +5C2O42-+16H+===2Mn2+ +10CO2↑+8H2O 增大 ab 探究其他离子浓度不变,溶液中H+浓度对反应速率的影响 ad
【解析】
(1)酸性条件下高锰酸根离子和草酸根离子发生氧化还原反应,根据元素守恒知,生成物中生成水,该反应中Mn元素化合价由+7价变为+2价、C元素化合价由+3价变为+4价,根据转移电子守恒、原子守恒配平方程式。
(2)一般来说,其他条件相同时,增大反应物浓度,反应速率增大。
(3)据MO变化趋势,得出反应速率随着草酸浓度增加而减小,可能原因是KMnO4与H2C2O4反应是分步进行的,反应过程中生成Mn(VI)、Mn(III)、Mn(IV),最终变为无色的Mn(II),以及草酸根易与不同价态锰离子形成较稳定的配位化合物,据此进行分析。
(4)小组进行实验III的目的是探究其他离子浓度不变,溶液中H+浓度对反应速率的影响。
(5)当草酸浓度较小时,C2O42﹣起主要作用,草酸浓度越大,反应速率越小;当草酸浓度较大时,H+起主要作用,使得草酸浓度越大,反应速率越大。
(1)酸性条件下高锰酸根离子和草酸根离子发生氧化还原反应,根据元素守恒知,生成物中有生成水,该反应中Mn元素化合价由+7价变为+2价、C元素化合价由+3价变为+4价,转移电子数为10,根据转移电子守恒、原子守恒配平方程式得2MnO4﹣+5C2O42﹣+16H+=2Mn2++10CO2↑+8H2O,故答案为:2MnO4﹣+5C2O42﹣+16H+=2Mn2++10CO2↑+8H2O。
(2)一般来说,其他条件相同时,增大反应物浓度,反应速率增大,故答案为:增大。
(3)MO变化趋势,得出反应速率随着草酸浓度增加而减小,可能原因是KMnO4与H2C2O4反应是分步进行的,反应过程中生成Mn(VI)、Mn(III)、Mn(IV),最终变为无色的Mn(II),以及草酸根易与不同价态锰离子形成较稳定的配位化合物。
故答案为:ab。
(4)小组进行实验III的目的是探究其他离子浓度不变,溶液中H+浓度对反应速率的影响,
故答案为:探究其他离子浓度不变,溶液中H+浓度对反应速率的影响。
(5)当草酸浓度较小时,C2O42﹣起主要作用,草酸浓度越大,反应速率越小;当草酸浓度较大时,H+起主要作用,使得草酸浓度越大,反应速率越大。故选ad。

 新思维寒假作业系列答案
新思维寒假作业系列答案【题目】Bodensteins研究反应H2(g)+I2(g)![]() 2HI(g),温度为T时,在两个体积均为1 L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w (HI)与反应时间t的关系如下表:
2HI(g),温度为T时,在两个体积均为1 L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w (HI)与反应时间t的关系如下表:
容器编号 | 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
I | 0.5 mol I2、0.5 mol H2 | w (HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
II | x mol HI | w (HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
研究发现上述反应中:v正=ka·w(H2)·w(I2),v逆=kb·w2(HI),其中ka、kb为常数。下列说法正确的是:
A. 温度为T时,该反应![]()
B. 容器I中在前20 min的平均速率v(HI)=0.0125 mol·L-1·min-1
C. 若起始时向容器I中加入物质的量均为0.1 mol的H2、I2、HI,反应逆向进行
D. 若两容器中存在kaⅠ= kaⅡ且kbⅠ= kbⅡ,则x的值可以为任何值