题目内容
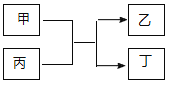
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下,下列说法错误的是 ( )
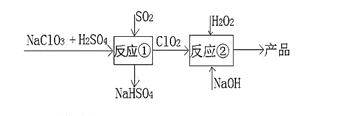
A.反应①阶段,参加反应的 NaClO3 和 SO2 的物质的量之比为 2:1
B.反应②中的 H2O2 可以用 NaClO4 代替
C.反应②条件下,ClO2 的氧化性大于 H2O2
D.根据流程信息,可推测 NaClO3 氧化性强于 NaClO2
【答案】B
【解析】
A. 反应①阶段,反应方程式为2NaClO3+SO2+H2SO4=2ClO2↑+2NaHSO4,则参加反应的 NaClO3 和 SO2 的物质的量之比为 2:1,A正确;
B. 反应②方程式为2ClO2+H2O2+2NaOH=2NaClO2+O2+2H2O,在此反应中,H2O2 作还原剂,而 NaClO4 中Cl达到了最高化合价,不能作还原剂,B错误;
C. 由反应②可得出,ClO2 的氧化性大于 H2O2,C正确;
D. 根据两个反应提供的信息,可推测氧化性 NaClO3>ClO2>NaClO2,D正确。
故选B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目