题目内容
已知下列反应:
Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O
2FeCl3+2KI═2FeCl2+I2+2KCl Cl2+2FeCl2═2FeCl3
则下列物质氧化性由强到弱的顺序是( )
Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O
2FeCl3+2KI═2FeCl2+I2+2KCl Cl2+2FeCl2═2FeCl3
则下列物质氧化性由强到弱的顺序是( )
| A、I2>FeCl3>Cl2>Co2O3 |
| B、Co2O3>Cl2>FeCl3>I2 |
| C、Cl2>Co2O3>I2>FeCl3 |
| D、Cl2>I2>Co2O3>FeCl3 |
考点:氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性.
解答:
解:在Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O中,氧化剂是Co2O3,氧化产物是Cl2,所以氧化性Co2O3>Cl2;在2FeCl3+2KI═2FeCl2+I2+2KCl中,氧化剂是FeCl3,氧化产物是I2,所以氧化性FeCl3>I2;在Cl2+2FeCl2═2FeCl3中,氧化剂是Cl2,氧化产物是FeCl3,所以氧化性Cl2>FeCl3;
故氧化性由强到弱的顺序是:Co2O3>Cl2>FeCl3>I2,
故选B.
故氧化性由强到弱的顺序是:Co2O3>Cl2>FeCl3>I2,
故选B.
点评:本题考查氧化性强弱的判断,难度不大.要注意在氧化还原反应中:氧化剂的氧化性强于氧化产物的氧化性.

练习册系列答案
相关题目
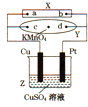 如图中X为电源,Y为浸透饱和硫酸钠溶液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散,下列判断正确的是( )
如图中X为电源,Y为浸透饱和硫酸钠溶液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散,下列判断正确的是( )| A、c电极的电极反应式为:2H++2e-=H2↑ |
| B、Cu电极质量减小,Pt电极质量增大 |
| C、Z中溶液的pH先减小,后增大 |
| D、a为电源正极,b为电源负极 |
下列各溶液中,物质的量浓度关系正确的是( )
| A、在0.1mol?L-1 CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) |
| B、0.1mol?L-1的KAl(SO4)2溶液中:c(SO42-)>c(Al3+)>c(OH-)>c(H+) |
| C、pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有:c(NaOH)<c(CH3COONa)<c(NaHCO3) |
| D、等体积、等物质的量浓度的NaX和弱碱HX混合后的溶液,若溶液呈酸性,则有c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是( )
| A、氧化铁、硫酸铜、硫酸 |
| B、氢氟酸、空气、纯碱 |
| C、硝酸、胆矾、熟石灰 |
| D、醋酸、食盐水、烧碱 |
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A、常温常压下,28g N2所含有的原子数目为2NA |
| B、42g C2H4和C3H6的混合物中原子数为3NA |
| C、12g金刚石中的C-C键数目为4NA个 |
| D、标准状况下,NA个H2O占有的体积为22.4L |
下列数量的各物质所含原子个数由大到小顺序排列的是( )
①0.5mol氨气 ②4g氦气 ③4℃时9mL水 ④0.2mol磷酸钠.
①0.5mol氨气 ②4g氦气 ③4℃时9mL水 ④0.2mol磷酸钠.
| A、④③②① | B、①④③② |
| C、②③④① | D、①④②③ |
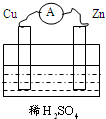 如图将Cu、Zn两种金属片插入稀H2SO4中,构成铜锌原电池,下列关于铜锌原电池的叙述正确的是( )
如图将Cu、Zn两种金属片插入稀H2SO4中,构成铜锌原电池,下列关于铜锌原电池的叙述正确的是( )| A、溶液中的H+向负极移动 |
| B、Zn片作负极,发生还原反应 |
| C、溶液的PH值将增大 |
| D、电子从Cu流出经导线流向Zn |