题目内容
(1)下列两组无色溶液分别选用一种试剂鉴别,写出试剂的化学式
①NaCl、Na2CO3、Na2SiO3 试剂: ;
②MgCl2、AlCl3、CuCl2、FeCl3 试剂: ;
(2)下列物质中含有少量杂质(括号内物质为杂质),用离子方程式表示除去杂质的原理.
①NaHCO3(Na2CO3)离子方程式 ;
②SiO2(CaCO3)离子方程式 ;
③Fe2O3(Al2O3)离子方程式 ;
(3)保存氢氧化钠溶液不可用磨口玻璃瓶塞(离子方程式) ;
(4)将氢氧化亚铁置于空气中,观察到白色沉淀迅速变为灰绿色,最后变为红褐色,写出反应的化学方程式 .
①NaCl、Na2CO3、Na2SiO3 试剂:
②MgCl2、AlCl3、CuCl2、FeCl3 试剂:
(2)下列物质中含有少量杂质(括号内物质为杂质),用离子方程式表示除去杂质的原理.
①NaHCO3(Na2CO3)离子方程式
②SiO2(CaCO3)离子方程式
③Fe2O3(Al2O3)离子方程式
(3)保存氢氧化钠溶液不可用磨口玻璃瓶塞(离子方程式)
(4)将氢氧化亚铁置于空气中,观察到白色沉淀迅速变为灰绿色,最后变为红褐色,写出反应的化学方程式
考点:物质的检验和鉴别的基本方法选择及应用,物质的分离、提纯的基本方法选择与应用
专题:物质检验鉴别题,化学实验基本操作
分析:(1)①NaCl、Na2CO3、Na2SiO3分别与盐酸反应的现象为:无现象、气体生成、白色沉淀生成;
②MgCl2、AlCl3、CuCl2、FeCl3分别与NaOH反应的现象为:白色沉淀、先生成白色沉淀后溶解、蓝色沉淀、红褐色沉淀;
(2)①Na2CO3与二氧化碳、水反应生成碳酸氢钠;
②CaCO3与盐酸反应,二氧化硅不能;
③Al2O3与NaOH反应,氧化铁不能;
(3)二氧化硅与NaOH溶液反应生成具有粘合性的硅酸钠;
(4)氢氧化亚铁与氧气、水反应生成氢氧化铁.
②MgCl2、AlCl3、CuCl2、FeCl3分别与NaOH反应的现象为:白色沉淀、先生成白色沉淀后溶解、蓝色沉淀、红褐色沉淀;
(2)①Na2CO3与二氧化碳、水反应生成碳酸氢钠;
②CaCO3与盐酸反应,二氧化硅不能;
③Al2O3与NaOH反应,氧化铁不能;
(3)二氧化硅与NaOH溶液反应生成具有粘合性的硅酸钠;
(4)氢氧化亚铁与氧气、水反应生成氢氧化铁.
解答:
解:(1)①NaCl、Na2CO3、Na2SiO3分别与盐酸反应的现象为:无现象、气体生成、白色沉淀生成,现象不同,可鉴别,故答案为:HCl;
②MgCl2、AlCl3、CuCl2、FeCl3分别与NaOH反应的现象为:白色沉淀、先生成白色沉淀后溶解、蓝色沉淀、红褐色沉淀,现象不同,可鉴别,故答案为:NaOH;
(2)①Na2CO3与二氧化碳、水反应生成碳酸氢钠,则除杂的离子反应为CO32-+CO2+H2O=HCO3-,故答案为:CO32-+CO2+H2O=HCO3-;
②CaCO3与盐酸反应,二氧化硅不能,则除杂的离子反应为CaCO3+2H+=Ca2++CO2+H2O,故答案为:CaCO3+2H+=Ca2++CO2+H2O;
③Al2O3与NaOH反应,氧化铁不能,则除杂的离子反应为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O;
(3)保存氢氧化钠溶液不可用磨口玻璃瓶塞,是因二氧化硅与NaOH溶液反应生成具有粘合性的硅酸钠,离子反应为SiO2+2OH-=SiO32-+H2O,故答案为:SiO2+2OH-=SiO32-+H2O;
(4)氢氧化亚铁与氧气、水反应生成氢氧化铁,发生的化学反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
②MgCl2、AlCl3、CuCl2、FeCl3分别与NaOH反应的现象为:白色沉淀、先生成白色沉淀后溶解、蓝色沉淀、红褐色沉淀,现象不同,可鉴别,故答案为:NaOH;
(2)①Na2CO3与二氧化碳、水反应生成碳酸氢钠,则除杂的离子反应为CO32-+CO2+H2O=HCO3-,故答案为:CO32-+CO2+H2O=HCO3-;
②CaCO3与盐酸反应,二氧化硅不能,则除杂的离子反应为CaCO3+2H+=Ca2++CO2+H2O,故答案为:CaCO3+2H+=Ca2++CO2+H2O;
③Al2O3与NaOH反应,氧化铁不能,则除杂的离子反应为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O;
(3)保存氢氧化钠溶液不可用磨口玻璃瓶塞,是因二氧化硅与NaOH溶液反应生成具有粘合性的硅酸钠,离子反应为SiO2+2OH-=SiO32-+H2O,故答案为:SiO2+2OH-=SiO32-+H2O;
(4)氢氧化亚铁与氧气、水反应生成氢氧化铁,发生的化学反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评:本题考查较综合,涉及物质的检验、分离提纯及除杂等,注重高频考点的考查,把握物质的性质及发生的反应、混合物的分离方法为解答的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
举世闻名的秦兵马俑制品的主要材料在成分上属于( )
| A、氧化铝 | B、二氧化硅 |
| C、硅酸盐 | D、合金 |
已知下列反应:
Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O
2FeCl3+2KI═2FeCl2+I2+2KCl Cl2+2FeCl2═2FeCl3
则下列物质氧化性由强到弱的顺序是( )
Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O
2FeCl3+2KI═2FeCl2+I2+2KCl Cl2+2FeCl2═2FeCl3
则下列物质氧化性由强到弱的顺序是( )
| A、I2>FeCl3>Cl2>Co2O3 |
| B、Co2O3>Cl2>FeCl3>I2 |
| C、Cl2>Co2O3>I2>FeCl3 |
| D、Cl2>I2>Co2O3>FeCl3 |
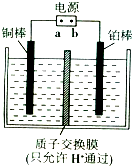 工业上将烟气中的二氧化硫转化为硫,常用的两种方法分别是热解气还原法和离子膜电解法.
工业上将烟气中的二氧化硫转化为硫,常用的两种方法分别是热解气还原法和离子膜电解法.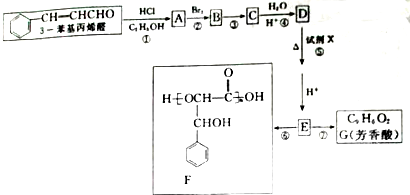
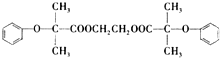 )可由下列路线合成:
)可由下列路线合成: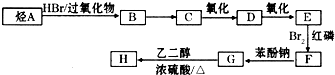

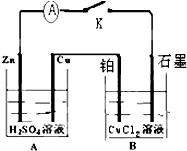 如图,回答问题:
如图,回答问题: