题目内容
7.若NA为阿伏伽德罗常数,则3.4g氨气中所含氢原子个数为0.6NA.分析 根据n=$\frac{m}{M}$计算出氨气的物质的量,再根据N=nNA计算出含有氨气分子含有的氢原子数目.
解答 解:氨气的相对分子质量是17,其摩尔质量是17g/mol,则3.4g氨气的物质的量为:n(NH3)=$\frac{3.4g}{17g/mol}$=0.2mol,所以含有氨气的分子数为:N(NH3)=nNA=0.2×NA=0.2NA,含有氢原子的数目为:N(H)=3N(NH3)=0.6NA,
故答案为:0.6NA.
点评 本题考查了有关物质的量的计算,题目难度不大,注意掌握物质的量与阿伏伽德罗常数、摩尔质量、物质的量浓度等物理量之间的转化关系.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
17.在测定中和热的实验中,下列说法中正确的是( )
| A. | 该实验需要用的主要玻璃仪器有:两个大小相同的烧杯、两只大小相同的量筒、温度计、环形玻璃搅拌棒 | |
| B. | 能用保温杯代替烧杯做有关测定中和热的实验 | |
| C. | 该实验至少需要测定并记录温度的次数是3次 | |
| D. | 若NaOH的物质的量稍大于HCl,会导致所测中和热数值偏高 |
18.重铬酸钠(Na2Cr2O7•2H2O)俗称红矾钠,在工业上有广泛的用途.我国目前主要是以铬铁矿(主要成份为FeO•Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下:
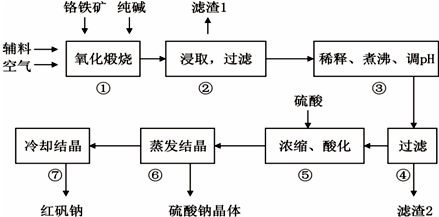
①中涉及的主要反应有:
主反应:4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$ 8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$ Na2SiO3+CO2↑、Al2O3+Na2CO3$\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
试回答下列问题:
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是使反应物接触更充分,加快反应速率.
(2)“③”中调节pH至4.7,目的是除去溶液中的AlO2-、SiO32-.
(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式:2CrO42-+2H+?Cr2O72-+H2O.
(4)“⑦”中采用冷却结晶的方法析出红矾钠,依据是红矾钠的溶解度随温度的降低而减小.
(5)制取红矾钠后的废水中还含有少量的CrO42-,根据有关标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol•L-1以下才能排放.含CrO42-的废水处理通常有以下两种方法.
①沉淀法:加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+.加入可溶性钡盐后的废水中Ba2+的浓度应不小于2.4×10-4mol•L-1,后续废水处理方能达到排放标准.
②还原法:CrO42-$\underset{\stackrel{绿矾}{→}}{{H}^{+}}$Cr3+$\stackrel{石灰水}{→}$Cr(OH)3.绿矾还原CrO42-的离子方程式为:Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O.
用该方法处理10m3 CrO42-的物质的量浓度为1.5×10-3 mol•L-1的废水,至少需要绿矾(FeSO4•7H2O,相对分子质量为278)的质量是12.51Kg.

①中涉及的主要反应有:
主反应:4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$ 8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$ Na2SiO3+CO2↑、Al2O3+Na2CO3$\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| 完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是使反应物接触更充分,加快反应速率.
(2)“③”中调节pH至4.7,目的是除去溶液中的AlO2-、SiO32-.
(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式:2CrO42-+2H+?Cr2O72-+H2O.
(4)“⑦”中采用冷却结晶的方法析出红矾钠,依据是红矾钠的溶解度随温度的降低而减小.
(5)制取红矾钠后的废水中还含有少量的CrO42-,根据有关标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol•L-1以下才能排放.含CrO42-的废水处理通常有以下两种方法.
①沉淀法:加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+.加入可溶性钡盐后的废水中Ba2+的浓度应不小于2.4×10-4mol•L-1,后续废水处理方能达到排放标准.
②还原法:CrO42-$\underset{\stackrel{绿矾}{→}}{{H}^{+}}$Cr3+$\stackrel{石灰水}{→}$Cr(OH)3.绿矾还原CrO42-的离子方程式为:Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O.
用该方法处理10m3 CrO42-的物质的量浓度为1.5×10-3 mol•L-1的废水,至少需要绿矾(FeSO4•7H2O,相对分子质量为278)的质量是12.51Kg.
19.常温下将一定浓度的某一元酸HA和0.1mol/L NaOH溶液等体积混合后,下列说法正确的是( )
| A. | 若pH=7,c(HA)=0.1 mol/L | |
| B. | 若pH<7,微粒浓度关系可能为:c(Na+)=c(HA)+c(A-) | |
| C. | 若pH>7,c(A-)>c(Na+) | |
| D. | 若pH=12,且HA为强酸时,c(HA)=0.08 mol/L |
16.下面关于电解质的叙述中正确的是( )
| A. | 在水溶液中或熔融状态下均不导电的化合物叫非电解质 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | 电解质在水中一定能导电,在水中导电的化合物一定是电解质 | |
| D. | 纯水的导电性很差,所以水不是电解质 |
 根据下式所示的氧化还原反应设计一个原电池:Fe+2Fe3+═3Fe2+
根据下式所示的氧化还原反应设计一个原电池:Fe+2Fe3+═3Fe2+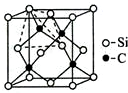 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.回答下列问题:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.回答下列问题: