题目内容
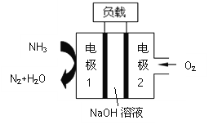
【题目】某氨气燃料电池,如图所示,下列说法不正确的是
A.正极的电极反应式为O2+4e-+4H+=2H2O
B.电子流向:电极1→负载→电极2
C.Na+由左向右移动
D.NH3在电极1上发生氧化反应
【答案】A
【解析】
该电池中氨气转化为氮气发生氧化反应,所以通入氨气的一极为负极,通入氧气的一极为正极。
A.通入氧气的一极为正极,电解质溶液为碱性,所以氧气得电子生成氢氧根,电极方程式为O2+4e-+2H2O=4OHˉ,故A错误;
B.原电池中电子由负极经导线流向正极,根据分析可知电极1为负极,电极2为正极,所以电子的流向为电极1→负载→电极2,故B正确;
C.原电池中阳离子流向正极,所以钠离子自左向右移动,故C正确;
D.据图可知NH3在电极1上转化为N2和H2O,失电子发生氧化反应,故D正确;
故答案为A。

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目