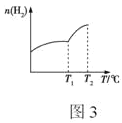
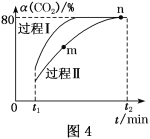
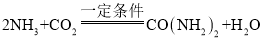题目内容
【题目】现有甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素(仅一个条件改变)。甲小组有如下实验设计方案。
实验编号 | 温度 | 催化剂 | 浓度 |
甲组实验Ⅰ | 25℃ | 三氧化二铁 | 10mL 5%H2O2 |
甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
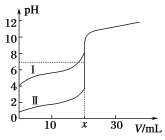
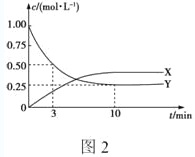
甲、乙两小组得出如图数据:
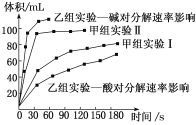
关于该实验下列叙述不正确的是
A. 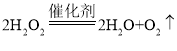 中,O2是氧化产物
中,O2是氧化产物
B. 甲小组实验得出的结论是Fe2O3比MnO2催化效率更高
C. 甲小组实验也可以测定25℃时,在相同时间内产生氧气的体积
D. 乙组研究的影响因素的数据分析,相同条件下H2O2在碱性环境下放出气体速率较快
【答案】B
【解析】
A.该反应中,氧元素的化合价既升高又降低,氧气是化合价升高的结果,所以是氧化产物,故A不选;
B. 从图中可以看出,MnO2可以使反应速率更快,所以Fe2O3比MnO2催化效率低,故B错误,选B;
C. 在相同时间内产生氧气的体积也可以判断催化剂的催化效率,故C不选;
D. 从图中可以看出,相同条件下H2O2在碱性环境下放出气体速率较快,故D不选;
故选B。

【题目】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等 |
B元素原子的核外p电子数比s电子数少1 |
C原子第一至第四电离能如下: I1=738 kJ·mol-1,I2=1451 kJ·mol-1,I3=7733 kJ·mol-1,I4=10540 kJ·mol-1 |
D原子核外所有p轨道全满或半满 |
E元素的主族序数与周期数的差为4 |
F是前四周期中电负性最小的元素 |
G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
![]() ,该同学所画的电子排布图违背了____________。
,该同学所画的电子排布图违背了____________。
(4)G位于第_____族_____区,该元素的核外电子排布式为_____________________________。
(5)检验F元素的方法是____________。
【题目】写出下列有机物的系统命名或结构简式:
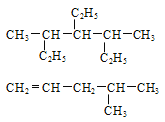
(1)_____________
(2)_____________
(3)4,4,5-三甲基-2-己炔 _______________
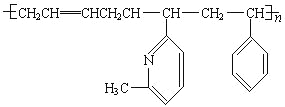
(4)新型弹性材料“丁苯吡橡胶”的结构简式如下:其单体为______________(有几种写几种)
(5)如下表所示,为提纯下列物质(括号内为少量杂质),填写所选用的除杂试剂与主要分离方法
不纯物质 | 除杂试剂 | 分离方法 | |
1 | 溴苯(Br2) | __________ | __________ |
2 | 乙醛(乙酸) | __________ | __________ |
3 | 乙酸乙酯(乙酸) | __________ | __________ |
4 | 乙醇(苯酚) | __________ | __________ |
5 | 硝基苯(硝酸) | __________ | __________ |
(6)①C5H12O的醇,在一定条件下能发生催化氧化反应,产物能与新制的氢氧化铜反应生成红色沉淀,醇的核磁共振氢谱中有三组峰,写出满足上述条件的醇的结构简式______
②C5H12O的醇,在一定条件下不能发生消去反应,写出满足条件的醇的结构简式______
③分子式为C5H12O,不能与金属钠反应.核磁共振氢谱中有四组峰,峰的面积比为3:2:1:6,写出满足上述条件的物质的结构简式______.