题目内容
【题目】回答有关问题:
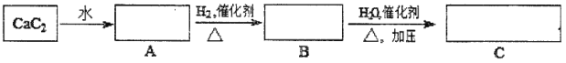
(1)A→B的反应类型是___________,实验室制取B的反应条件是________________。
(2)A和氯化氢为原料可以制得塑料聚氯乙烯。写出制备过程中最后一步发生的方程式:__________。
【答案】加成反应 浓硫酸、170℃ nCH2=CH-Cl![]()
![]()
【解析】
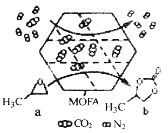
由流程图可知CaC2与水反应生成Ca(OH)2和C2H2,由A与氢气发生加成反应生成B可知,A为C2H2,由B能与H2O发生加成反应生成C可知,B为C2H4,C为CH3CH2OH,据此解答。
由流程图可知CaC2与水反应生成Ca(OH)2和C2H2,由A与氢气发生加成反应生成B可知,A为C2H2,由B能与H2O发生加成反应生成C可知,B为C2H4,C为CH3CH2OH;
(1)C2H2与氢气发生反应生成C2H4的反应类型是加成反应;实验室用乙醇在浓硫酸作催化剂、170℃条件下制取C2H4;故答案为:加成反应;浓硫酸、170℃;
(2)C2H2和氯化氢为原料可以制得塑料聚氯乙烯,首先用C2H2和氯化氢发生加成反应生成氯乙烯,然后氯乙烯发生加聚反应生成聚氯乙烯,化学方程式为:nCH2=CH-Cl![]()
![]() ;故答案为:nCH2=CH-Cl
;故答案为:nCH2=CH-Cl![]()
![]() 。
。

练习册系列答案
相关题目
【题目】实验室用浓度为0.500mol/L的标准氢氧化钠溶液来测定未知浓度的盐酸。在锥形瓶中放入20.00mL的待测溶液,再滴加2滴酚酞,摇匀。用标准氢氧化钠溶液滴定,直到滴入最后一滴氢氧化钠溶液,指示剂的颜色_______,并在半分钟内溶液颜色不发生变化,停止滴定,记录读数。数据如表:
次数 | 滴定前(mL) | 滴定后(mL) |
1 | 0.40 | 21.10 |
2 | 0.10 |
第2次滴定后滴定管的读数如图所示。根据表中的数据计算出盐酸的浓度为_____mol/L。