题目内容
20. 镍及其化合物常用作合金、催化剂及电极材料.已知:镍元素有+2、+3价的氧化物和氢氧化物,在盐中以+2价的形式存在.
镍及其化合物常用作合金、催化剂及电极材料.已知:镍元素有+2、+3价的氧化物和氢氧化物,在盐中以+2价的形式存在.(1)镍与稀硝酸反应放出NO,反应的化学方程式是3Ni+8HNO3=3Ni(NO3)2+2NO↑+4H2O.
(2)Ni2O3是一种重要的电池材料.
①铁镍蓄电池放电时总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2
电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2;
电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+6H2O.
②在碱性条件下,镍氢电池的总反应为:3Ni2O3+LaNi5H6+3H2O$?_{充电}^{放电}$LaNi5+6Ni(OH)2,该电池放电时,负极电极反应为LaNi5H6+6OH--6e-=LaNi5+6H2O
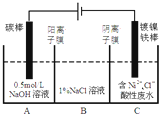
(3)工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.
已知:
①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
下列说法不正确的是BD
A.碳棒上发生的电极反应:4OH--4e- O2↑+2H2O
B.电解过程中,B室中NaCl溶液的物质的量浓度将不断减少
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式不发生改变
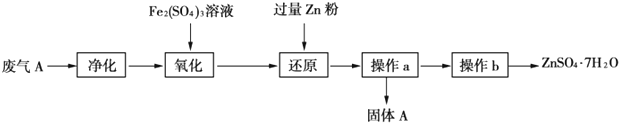
(4)某工厂用废的含镍催化剂(主要含Ni,还含有一定量的Al、Fe、SiO2)回收镍的流程如下:

已知:上述流程中,几种氢氧化物完全沉淀时的pH如下表:
| 沉淀 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
②滤渣b所含成份的化学式为Al(OH)3、Fe(OH)3.
③若将溶液调整为pH=6时加入了bkgNi(OH)2,从酸浸到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,akg废催化剂(含Ni70%)经上述流程最终得到金属镍的质量为(a×70%×97%+$\frac{59}{93}$b)×95%kg(填计算式).
分析 (1)镍与稀硝酸反应放出NO,同时生成硫酸镍,根据元素守恒可写出化学方程式;
(2)①根据电池的总反应:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2,放电时Fe作负极,发生氧化反应失电子生成Fe2+,最终生成Fe(OH)2;Ni2O3作正极,发生还原反应,得电子,最终生成Ni(OH)2,电池充电时,阳极Ni(OH)2发生氧化反应生成Ni2O3,据此分析;
②电池放电时的反应为LaNi5H6+6NiO(OH)═LaNi5+6Ni(OH)2,该电池放电时,负极NiOOH发生氧化反应生成Ni(OH)2,根据电荷守恒和元素守恒可写出电极反应式;
(3)A、由图分析可知,碳棒与电源正极相连是电解池的阳极,电极反应4OH--4e-=2H2O+O2↑;
B、镀镍铁棒与电源负极相连是电解池的阴极,电极反应Ni2++2e-=Ni.电解过程中为平衡A、C中的电荷,A中的Na+和C中的Cl-分别通过阳离子膜和阴离子膜移向B中,这使B中NaCl溶液的物质的量浓度不断增大;
C、因Ni2+在弱酸性溶液中易发生水解,氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度),为了提高Ni的产率,电解过程中需要控制废水pH;
D、若将图中阳离子膜去掉,由于放电顺序Cl->OH-,则Cl-移向阳极放电:2Cl- --2e-=Cl2↑,电解反应总方程式会发生改变;
(4)废镍催化剂(主要含Ni,还含有一定量的Al、Fe、SiO2),用硫酸溶解,SiO2不与硫酸反应,过滤得到滤液A中含有NiSO4、FeSO4、Al2(SO4)3及过量的硫酸,加入 的是H2O2将Fe2+氧化为Fe3+,加入Ni(HO)2调节pH为6,使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀,过滤得滤渣b为Al(OH)3、Fe(OH)3,滤液中含有NiSO4,将滤液pH值调到9.2,使镍离子沉淀,再加N2H4•H2O还原得金属镍,据此答题.
解答 解:(1)镍与稀硝酸反应放出NO,同时生成硫酸镍,反应的化学方程式为3Ni+8HNO3=3Ni(NO3)2+2NO↑+4H2O,
故答案为:3Ni+8HNO3=3Ni(NO3)2+2NO↑+4H2O;
(2)①根据电池的总反应:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2,放电时Fe作负极,发生氧化反应失电子生成Fe2+,最终生成Fe(OH)2,负极电极反应式为Fe+2OH--2e-=Fe(OH)2,Ni2O3作正极,发生还原反应,得电子,最终生成Ni(OH)2,电极反应式为,电池充电时,阳极Ni(OH)2发生氧化反应生成Ni2O3,电极反应式为2Ni(OH)2+2OH--2e-=Ni2O3+6H2O,
故答案为:Fe+2OH--2e-=Fe(OH)2;2Ni(OH)2+2OH--2e-=Ni2O3+6H2O;
②电池放电时的反应为LaNi5H6+6NiO(OH)═LaNi5+6Ni(OH)2,该电池放电时,负极NiOOH发生氧化反应生成Ni(OH)2,电极反应式为LaNi5H6+6OH--6e-=LaNi5+6 H2O,
故答案为:LaNi5H6+6OH--6e-=LaNi5+6 H2O;
(3)A、由图知,碳棒与电源正极相连是电解池的阳极,电极反应4OH--4e-=2H2O+O2↑,故A正确;
B、镀镍铁棒与电源负极相连是电解池的阴极,电极反应Ni2++2e-=Ni.电解过程中为平衡A、C中的电荷,A中的Na+和C中的Cl-分别通过阳离子膜和阴离子膜移向B中,这使B中NaCl溶液的物质的量浓度不断增大,故B错误;
C、因Ni2+在弱酸性溶液中易发生水解;氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度),为了提高Ni的产率,电解过程中需要控制废水pH,故C正确;
D、若将图中阳离子膜去掉,由于放电顺序Cl->OH-,则Cl-移向阳极放电:2Cl- --2e-=Cl2↑,电解反应总方程式会发生改变,故D错误;
故选BD;
(4)废镍催化剂(主要含Ni,还含有一定量的Al、Fe、SiO2),用硫酸溶解,SiO2不与硫酸反应,过滤得到滤液A中含有NiSO4、FeSO4、Al2(SO4)3及过量的硫酸,加入 的是H2O2将Fe2+氧化为Fe3+,加入Ni(HO)2调节pH为6,使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀,过滤得滤渣b为Al(OH)3、Fe(OH)3,滤液中含有NiSO4,将滤液pH值调到9.2,使镍离子沉淀,再加N2H4•H2O还原得金属镍,
①水合肼(N2H4•H2O)是强还原剂,氧化产物对环境友好,由“沉淀→镍”的化学方程式为2Ni(OH)2+N2H4•H2O═2Ni+N2↑+5H2O,
故答案为:2Ni(OH)2+N2H4•H2O═2Ni+N2↑+5H2O;
②根据上面的分析可知,滤渣b所含成份的化学式为Al(OH)3、Fe(OH)3,
故答案为:Al(OH)3、Fe(OH)3;
③bkgNi(OH)2中镍元素的质量为$\frac{59}{93}$bkg,akg废催化剂(含Ni70%)中镍元素的质量为akg×70%,从酸浸到滤液B的过程中镍的损失率为3%,根据镍元素守恒可知,最终得到金属镍的质量为(a×70%×97%+$\frac{59}{93}$b)×95% kg,
故答案为:(a×70%×97%+$\frac{59}{93}$b)×95%.
点评 本题考查制备方案,涉及化学工艺流程、对操作与试剂的分析评价、化学方程式书写、原电池与电解原理等,是对学生综合能力的考查,需要学生具备扎实的基础与迁移运用能力,难度中等.

| A. | V1=V2 | B. | V1>V2 | C. | V1<V2 | D. | V1≤V2 |
(1)写出反应中涉及的化学方程式(至少3个)
(2)通过计算,填写下表:
| c(H+) | c(SO42-) | c(Fe2+、Fe3+) |
(3)计算原溶液中Fe2+被氧化的百分率.
A.氟利昂 B.SO2C.NO2D.CO2
| 环境问题 | 造成环境问题的主要物质 |
| 温室效应 | |
| 酸雨 | |
| 南极臭氧层空洞 | |
| 光化学烟雾 |
| A. | 将pH=4的盐酸和醋酸分别稀释成pH=5的溶液时所加水的量 | |
| B. | pH=10的NaOH和Na2CO3溶液中水的电离程度 | |
| C. | 相同温度下,10 mL 0.1mol/L的醋酸与100 mL 0.01mol/L的醋酸中H+的物质的量 | |
| D. | 物质的量浓度相等的(NH4)2SO4溶液与(NH4)2CO3溶液中NH${\;}_{4}^{+}$的物质的量浓度 |
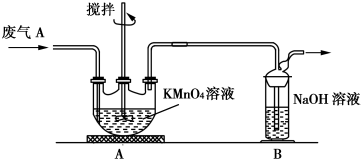
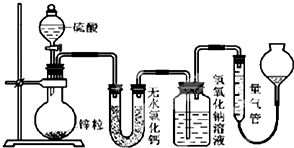 不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10lkPa,温度为0℃).
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10lkPa,温度为0℃).