题目内容
11.取等体积等浓度的氢氧化钠溶液两份,一份密封保存,另一份敞口放置.几天后,用相同浓度的盐酸分别去中和,至溶液中只有NaCl.若第一份用盐酸V1mL,第二份用盐酸为V2,则V1与V2关系正确的是( )| A. | V1=V2 | B. | V1>V2 | C. | V1<V2 | D. | V1≤V2 |
分析 氢氧化钠敞口放置,则2NaOH+CO2=Na2CO3+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑;氢氧化钠和盐酸反应生成氯化钠和水NaOH+HCl=NaCl+H2O,根据钠元素守恒、氯元素守恒计算二者消耗盐酸的体积.
解答 解:氢氧化钠敞口放置,则则2NaOH+CO2=Na2CO3+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑;氢氧化钠和盐酸反应生成氯化钠和水NaOH+HCl=NaCl+H2O,根据钠元素守恒,氢氧化钠中和碳酸钠中钠离子的物质的量是相等的,再和盐酸反应,都得到的是氯化钠溶液,n(Na+)=n(Cl-),根据氯元素守恒,所以二者消耗的盐酸的物质的量是相等的,即用相同浓度的盐酸的体积是一样多的.
故选A.
点评 本题考查学生元素化合物的性质以及方程式的计算知识,注意元素守恒思想在解题中的应用是关键,难度中等.

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
1.实验室制备氯气,检验是否收集满的正确方法是( )
| A. | 用手扇动收集的气体,有气味则已收集满 | |
| B. | 将润湿的淀粉-KI试纸接近瓶口,试纸变蓝则已收集满 | |
| C. | 将润湿的红色石蕊试纸伸入瓶内,试纸腿色则已收集满 | |
| D. | 将铁丝伸到瓶口,铁丝燃烧说明已收集满 |
19.下列各组离子在指定溶液中,可能大量共存的是( )
| A. | 澄清透明的溶液中:NH${\;}_{4}^{+}$,Na+,HSO${\;}_{3}^{-}$,Cr2O${\;}_{7}^{2-}$ | |
| B. | c(H+)=10-13mol•L-1的溶液中:Cl-,Br-,S2O${\;}_{3}^{2-}$,Na+ | |
| C. | 能使pH试纸变深蓝色的溶液中:K+,Na+,AlO${\;}_{2}^{-}$,HCO${\;}_{3}^{-}$ | |
| D. | 加入Al能放出H2的溶液中:NO${\;}_{3}^{-}$,K+,SO${\;}_{4}^{2-}$,Mg2+ |
6.有机物M(  )是-种重要的医药中间体,下列有关它的说法中正确的是( )
)是-种重要的医药中间体,下列有关它的说法中正确的是( )
 )是-种重要的医药中间体,下列有关它的说法中正确的是( )
)是-种重要的医药中间体,下列有关它的说法中正确的是( )| A. | M的分子式为C8H10O3 | |
| B. | 在浓硫酸存在下加热M,可得到酚类物质 | |
| C. | 等量的M分别与足量Na、NaHCO3反应时得到的气体物质的量比为1:1 | |
| D. | M既可使酸性高锰酸钾溶液褪色,又可使溴水褪色,反应原理相同. |
16.化学与科学、技术、社会、环境密切相关,下列有关说法中错误的是( )
| A. | 神舟九号升空时火箭发射的动力主要来源于化学能 | |
| B. | 队洁厕灵的主要成分是盐酸,不能与“84“消毒液混用 | |
| C. | 采用催化转换技术将汽车尾气中的N0x和CO转化为无毒气体 | |
| D. | 为了能增加水中氧气的含量,养金鱼用的自来水一般先在阳光下晒一段时间. |
3.钴是重要的战略金属元素,钴及其化合物在化工、机械、航空和军事等部门具有广泛的应用.以水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等杂质)制取CoC2O4的工艺流程如图1:
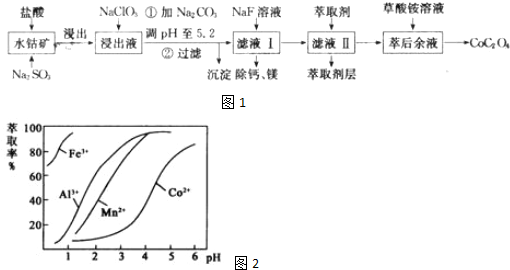
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)浸出过程中加入Na2SO3的目的是将Fe3+、Co3+(填离子符号)还原,若只用盐酸浸取,则会产生污染空气的有毒气体,反应的离子方程式为2Co3++2Cl-=Cl2 ↑+2Co2+.
(2)向浸出液中加入NaClO3的作用是将Fe2+氧化成Fe3+,反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O.
(3)浸出液中加Na2CO3调pH至5.2时生成的沉淀为Fe(OH)3、Al(OH)3(填化学式),能够生成此沉淀的原因是铝离子、铁离子能与碳酸根离子发生双水解生成沉淀和二氧化碳,反应的离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2、2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑(用离子方程式结合必要的文字说明).
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知KSp( MgF2)=7.35
×10-ll、Ksp( CaF2)=1.05×10-10,当加入过量NaF后,所得滤液中$\frac{c(M{g}^{2+})}{c(C{a}^{2+})}$=0.7
(5)滤液Ⅱ中加入萃取剂的作用是除去溶液中的Mn2+,萃取剂对金属离子的萃取率与pH的关系如图2所
示.使用萃取剂适宜的pH是B(填字母).
a.接近2.0
b.接近3.0
c.接近4.0.

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的目的是将Fe3+、Co3+(填离子符号)还原,若只用盐酸浸取,则会产生污染空气的有毒气体,反应的离子方程式为2Co3++2Cl-=Cl2 ↑+2Co2+.
(2)向浸出液中加入NaClO3的作用是将Fe2+氧化成Fe3+,反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O.
(3)浸出液中加Na2CO3调pH至5.2时生成的沉淀为Fe(OH)3、Al(OH)3(填化学式),能够生成此沉淀的原因是铝离子、铁离子能与碳酸根离子发生双水解生成沉淀和二氧化碳,反应的离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2、2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑(用离子方程式结合必要的文字说明).
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知KSp( MgF2)=7.35
×10-ll、Ksp( CaF2)=1.05×10-10,当加入过量NaF后,所得滤液中$\frac{c(M{g}^{2+})}{c(C{a}^{2+})}$=0.7
(5)滤液Ⅱ中加入萃取剂的作用是除去溶液中的Mn2+,萃取剂对金属离子的萃取率与pH的关系如图2所
示.使用萃取剂适宜的pH是B(填字母).
a.接近2.0
b.接近3.0
c.接近4.0.
20. 镍及其化合物常用作合金、催化剂及电极材料.已知:镍元素有+2、+3价的氧化物和氢氧化物,在盐中以+2价的形式存在.
镍及其化合物常用作合金、催化剂及电极材料.已知:镍元素有+2、+3价的氧化物和氢氧化物,在盐中以+2价的形式存在.
(1)镍与稀硝酸反应放出NO,反应的化学方程式是3Ni+8HNO3=3Ni(NO3)2+2NO↑+4H2O.
(2)Ni2O3是一种重要的电池材料.
①铁镍蓄电池放电时总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2
电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2;
电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+6H2O.
②在碱性条件下,镍氢电池的总反应为:3Ni2O3+LaNi5H6+3H2O$?_{充电}^{放电}$LaNi5+6Ni(OH)2,该电池放电时,负极电极反应为LaNi5H6+6OH--6e-=LaNi5+6H2O
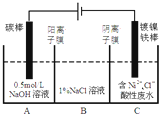
(3)工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.
已知:
①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
下列说法不正确的是BD
A.碳棒上发生的电极反应:4OH--4e- O2↑+2H2O
B.电解过程中,B室中NaCl溶液的物质的量浓度将不断减少
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式不发生改变
(4)某工厂用废的含镍催化剂(主要含Ni,还含有一定量的Al、Fe、SiO2)回收镍的流程如下:

已知:上述流程中,几种氢氧化物完全沉淀时的pH如下表:
①水合肼(N2H4•H2O)是强还原剂,氧化产物对环境友好.由“沉淀→镍”的化学方程式2Ni(OH)2+N2H4•H2O═2Ni+N2↑+5H2O.
②滤渣b所含成份的化学式为Al(OH)3、Fe(OH)3.
③若将溶液调整为pH=6时加入了bkgNi(OH)2,从酸浸到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,akg废催化剂(含Ni70%)经上述流程最终得到金属镍的质量为(a×70%×97%+$\frac{59}{93}$b)×95%kg(填计算式).
 镍及其化合物常用作合金、催化剂及电极材料.已知:镍元素有+2、+3价的氧化物和氢氧化物,在盐中以+2价的形式存在.
镍及其化合物常用作合金、催化剂及电极材料.已知:镍元素有+2、+3价的氧化物和氢氧化物,在盐中以+2价的形式存在.(1)镍与稀硝酸反应放出NO,反应的化学方程式是3Ni+8HNO3=3Ni(NO3)2+2NO↑+4H2O.
(2)Ni2O3是一种重要的电池材料.
①铁镍蓄电池放电时总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2
电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2;
电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+6H2O.
②在碱性条件下,镍氢电池的总反应为:3Ni2O3+LaNi5H6+3H2O$?_{充电}^{放电}$LaNi5+6Ni(OH)2,该电池放电时,负极电极反应为LaNi5H6+6OH--6e-=LaNi5+6H2O
(3)工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.
已知:
①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
下列说法不正确的是BD
A.碳棒上发生的电极反应:4OH--4e- O2↑+2H2O
B.电解过程中,B室中NaCl溶液的物质的量浓度将不断减少
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式不发生改变
(4)某工厂用废的含镍催化剂(主要含Ni,还含有一定量的Al、Fe、SiO2)回收镍的流程如下:

已知:上述流程中,几种氢氧化物完全沉淀时的pH如下表:
| 沉淀 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
②滤渣b所含成份的化学式为Al(OH)3、Fe(OH)3.
③若将溶液调整为pH=6时加入了bkgNi(OH)2,从酸浸到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,akg废催化剂(含Ni70%)经上述流程最终得到金属镍的质量为(a×70%×97%+$\frac{59}{93}$b)×95%kg(填计算式).
1.下列离子或分子能够在指定的分散系中大量共存的是( )
| A. | 铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH${\;}_{4}^{+}$、Cl-、NO${\;}_{3}^{-}$ | |
| B. | 澄清石灰水中:Na+、K+、CH3COO -、HCO${\;}_{3}^{-}$ | |
| C. | c(H+)=10-13mol/L的溶液中:NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、K+、Na+ | |
| D. | 空气中:SO2、NO、N2、NH3 |