题目内容
18.下列说法不正确的是( )| A. | 废旧电池应集中回收处理 | |
| B. | 充电电池放电时,化学能转变为电能 | |
| C. | 放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关 | |
| D. | 所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 |
分析 A.废旧电池含有汞镉等重金属;
B.原电池为化学能转化为电能装置;
C.升高温度可以加快反应速率,降低温度能够减慢反应速率;
D.可燃物燃烧时必须先达到着火点,即需要一定的能量.
解答 解:A.废旧电池含有汞镉等重金属,用完随便丢弃容易造成环境污染,应集中回收处理,故A正确;
B.充电电池放电时为原电池,原电池为化学能转化为电能装置,故B正确;
C.升高温度可以加快反应速率,降低温度能够减慢反应速率,冰箱内温度较低,放在冰箱中的食品保质期较长,故C正确;
D.有的燃烧反应是需要吸收一定热量才可以反应的,比如碳的燃烧,故D错误;
故选:D.
点评 本题考查了化学与生活,设计环境污染与治理、影响反应速率因素、反应热效应,掌握基础是解题关键,题目难度不大.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
9.将CH4跟Cl2混合,日光漫射,假设生成的4种氯代物的物质的量相等,则混合气体中CH4跟Cl2的物质的量比为( )
| A. | 1:4 | B. | 2:3 | C. | 1:7 | D. | 2:5 |
13.在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol•L-1、0.3mol•L-1、0.2mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A. | Z为0.3 mol•L-1 | B. | X2为0.2 mol•L-1 | ||
| C. | Y2为0.4 mol•L-1 | D. | c(X2)+c(Y2)+c(Z)=0.55 mol•L-1 |
3.下表是元素周期表的一部分,下列有关说法中正确的是( )
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | c | d | f | ||||
| 3 | a | b | e |
| A. | e的氢化物比d的氢化物稳定 | |
| B. | a~f六种元素中,相互之间最易形成离子键的是a和f | |
| C. | a~f六种元素中,原子半径最大的是e | |
| D. | 由a、d两种元素形成的离子化合物中,不可能含有共价键 |
10.向c(H+)相等的一元酸HA和HB的溶液中分别加入适量的锌粉,充分反应后,当收集到的H2体积相等时,消耗酸的体积V(HA)>V(HB),下列分析正确的是( )
| A. | 消耗锌的质量m(HA)>m(HB) | B. | HA一定是强酸 | ||
| C. | 生成H2的平均反应速率v(HA)<v(HB) | D. | 酸性:HB>HA |
7.一定温度下,在体积可变的恒温密闭容器中,甲醇在浓硫酸作催化剂的条件下发生下列反应:2CH3OH(g)=CH3OCH3(g)+H2O(g)△H=-25kJ•mol-1,下列有关该反应的叙述正确的是( )
| A. | 该条件下,1 mol CH3OH(g)参加反应,放出的热量为25 kJ | |
| B. | 若不采用合适的催化剂,该反应中甲醇的转化率将降低 | |
| C. | 升高温度和增大压强(缩小容器容积)均可加快反应速率 | |
| D. | 反应过程中,2v(CH3OH)=v(CH3OCH3) |
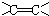 碳碳双键
碳碳双键  羰基
羰基 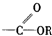 酯基.
酯基.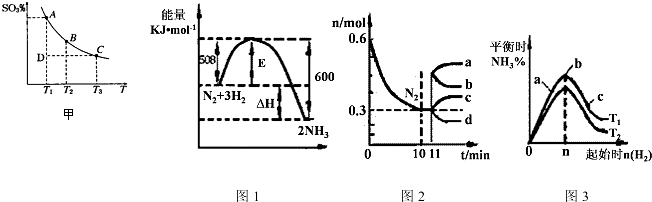
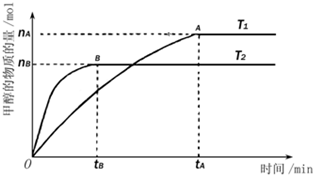 甲醇是一种新型的能源.
甲醇是一种新型的能源.