题目内容
3.下表是元素周期表的一部分,下列有关说法中正确的是( )族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | c | d | f | ||||
| 3 | a | b | e |
| A. | e的氢化物比d的氢化物稳定 | |
| B. | a~f六种元素中,相互之间最易形成离子键的是a和f | |
| C. | a~f六种元素中,原子半径最大的是e | |
| D. | 由a、d两种元素形成的离子化合物中,不可能含有共价键 |
分析 由元素在周期表中位置,可知a为Na、b为Mg、c为C、d为O、e为S、f为F.
A.同主族自上而下非金属性减弱,非金属性越强对应氢化物越稳定;
B.电负性相差最大,原子之间最易形成离子键;
C.同周期自左而右原子半径减小、同主族自上而下原子半径最大;
D.由a、d两种元素形成的离子化合物Na2O2中含有共价键.
解答 解:由元素在周期表中位置,可知a为Na、b为Mg、c为C、d为O、e为S、f为F.
A.同主族自上而下非金属性减弱,则非金属性d>e,非金属性越强对应氢化物越稳定,则e的氢化物不如d的氢化物稳定,故A错误;
B.同周期自左而右电负性增大、同主族自上而下电负性减小,故a、f电负性相差最大,原子之间最易形成离子键,故B正确;
C.同周期自左而右原子半径减小、同主族自上而下原子半径最大,故a的原子半径最大,故C错误;
D.由a、d两种元素形成的离子化合物Na2O2中含有共价键,故D错误,
故选:B.
点评 本题考查元素周期表与元素周期律综合应用,侧重对元素周期律的考查,难度不大,旨在考查学生对基础知识的掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.向 Cr2 (SO4)3 的水溶液中加入NaOH溶液,当pH=4.6时开始出现Cr(OH)3沉淀,随着pH的升高,沉淀增多,当pH≥13时,沉淀消失,出现亚铬酸根离子(CrO2-),其平衡关系:
Cr3++3OH-?Cr(OH)3?CrO2-+H++H2O
(紫色) (灰绿色) (亮绿色)
向50mL 0.05mol•L-1的Cr2(SO4)3 溶液中加入等体积1.0mol•L-1的 NaOH溶液,充分反应后,溶液中可观察到的现象为( )
Cr3++3OH-?Cr(OH)3?CrO2-+H++H2O
(紫色) (灰绿色) (亮绿色)
向50mL 0.05mol•L-1的Cr2(SO4)3 溶液中加入等体积1.0mol•L-1的 NaOH溶液,充分反应后,溶液中可观察到的现象为( )
| A. | 溶液为紫色 | B. | 溶液为亮绿色 | ||
| C. | 溶液中有灰绿色沉淀 | D. | 无法判断 |
14.下列物质常温下能与溴水发生取代反应的是( )
| A. | 苯酚 | B. | 苯乙烯(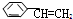 ) ) | C. | 苯 | D. | 苯甲醇(  ) ) |
11.下列说法正确的是( )
| A. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| B. | 同温同压下,H2 (g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 | |
| C. | 已知:①2H2(g)+O2(g)═2H2O(g)△H=-a kJ•mol-1,②2H2(g)+O2 (g)═2H2O(1)△H=-b kJ•mol-1,则a>b | |
| D. | 已知:①C(s,石墨)+O2 (g)═CO2(g)△H=-393.5 kJ•mol-1,②C(s,金刚石)+O2(g)═CO2 (g)△H=-395.0 kJ•mol-1,则C(s,石墨)═C(s,金刚石)△H=+1.5 kJ•mol-1 |
18.下列说法不正确的是( )
| A. | 废旧电池应集中回收处理 | |
| B. | 充电电池放电时,化学能转变为电能 | |
| C. | 放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关 | |
| D. | 所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 |
8.下列说法不正确的是( )
①FeCl3溶液可用于铜质印刷线路板制作是因为FeCl3能从含Cu2+的溶液中置换出铜
②室温下,不能将浓硫酸盛放在铁桶中
③K+、Fe3+、N${O}_{3}^{-}$、SCN-在水溶液中能大量共存
④因氧化铁能与酸反应,可用于制作红色涂料
⑤将Fe(NO)2样品溶于稀H2SO4后,滴加KSCN溶液观察溶液是否变红,可检验Fe(NO3)2晶体是否已氧化变质.
①FeCl3溶液可用于铜质印刷线路板制作是因为FeCl3能从含Cu2+的溶液中置换出铜
②室温下,不能将浓硫酸盛放在铁桶中
③K+、Fe3+、N${O}_{3}^{-}$、SCN-在水溶液中能大量共存
④因氧化铁能与酸反应,可用于制作红色涂料
⑤将Fe(NO)2样品溶于稀H2SO4后,滴加KSCN溶液观察溶液是否变红,可检验Fe(NO3)2晶体是否已氧化变质.
| A. | 仅①②③ | B. | 仅①③④ | C. | 仅②④⑤ | D. | 全部 |
15.工业生产水煤气的反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.4kJ•mol-1,下列判断正确的是( )
| A. | 反应物能量总和大于生成物能量总和 | |
| B. | CO(g)+H2(g)?C(s)+H2O(l)△H=-131.4kJ•mol-1 | |
| C. | 水煤气反应中生成1molH2(g)吸收131.4 kJ热量 | |
| D. | 水煤气反应中生成1L CO(g)吸收131.4 kJ热量 |
12.下列化学反应中,不属于四种基本反应类型的是( )
| A. | 2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑ | |
| B. | NH3+HCl═NH4Cl | |
| C. | Ba(OH)2+MgSO4═BaSO4↓+Mg(OH)2↓ | |
| D. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O |
13.假定元素周期表是有限的,根据已知的元素周期表的某些事实和理论可归纳出一些假说.

(1)已知元素周期表中的各周期可排元素种类如下:
人们预测元素周期表第八周期将来也会排满,那么该周期排满后的元素种数是50.
A.18 B.32 C.50 D.无法判断
(2)根据周期表中每个周期非金属元素的种数(把稀有气体元素看做非金属元素),预测周期表中应该有23种非金属元素,还有1种未发现.未发现的非金属元素处于七周期0族.
(3)小明同学所在的化学探究小组,在查阅相关资料后归纳出元素周期表的另一种画法--三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置.
回答下列问题:
①请在图中将过渡元素所在的位置涂黑.
②画出B元素价电子排布图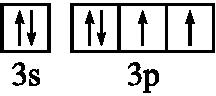 .
.

(1)已知元素周期表中的各周期可排元素种类如下:
| 周期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素种类 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
A.18 B.32 C.50 D.无法判断
(2)根据周期表中每个周期非金属元素的种数(把稀有气体元素看做非金属元素),预测周期表中应该有23种非金属元素,还有1种未发现.未发现的非金属元素处于七周期0族.
(3)小明同学所在的化学探究小组,在查阅相关资料后归纳出元素周期表的另一种画法--三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置.
回答下列问题:
①请在图中将过渡元素所在的位置涂黑.
②画出B元素价电子排布图
 .
.