题目内容
(12分)
某化学研究性学习小组开展实验探究:在常温下某非金属氧化物形成的未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清。由此该小组成员对气体的成分提出猜想。
【提出猜想】
猜想1:气体可能为CO2; 猜想2: ;
猜想3: 。
为了验证猜测,该小组设计实验加以探究:
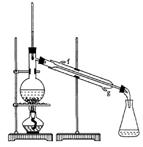
【实验探究】该小组按如图所示装置,将气体从a端通入,则:
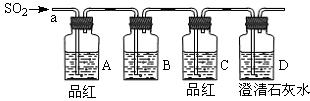
(1)B中应该装入下列 试剂(填编号)
(2)A中品红的作用是: ;
(3)D中澄清石灰水的作用是: 。
通过该实验,小组同学观察到以下三个实验现象:
① A中品红褪色 ② C中品红不褪色 ③ D中澄清石灰水变浑浊
【得出结论】由上述现象小组同学确认该气体的成分是 。
某化学研究性学习小组开展实验探究:在常温下某非金属氧化物形成的未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清。由此该小组成员对气体的成分提出猜想。
【提出猜想】
猜想1:气体可能为CO2; 猜想2: ;
猜想3: 。
为了验证猜测,该小组设计实验加以探究:
【实验探究】该小组按如图所示装置,将气体从a端通入,则:

(1)B中应该装入下列 试剂(填编号)
| A.NaCl溶液 | B.酸性KMnO4溶液 | C.盐酸 | D.澄清石灰水 |
(3)D中澄清石灰水的作用是: 。
通过该实验,小组同学观察到以下三个实验现象:
① A中品红褪色 ② C中品红不褪色 ③ D中澄清石灰水变浑浊
【得出结论】由上述现象小组同学确认该气体的成分是 。
(12分)
【提出猜想】
猜想2:气体可能为SO2(2分);猜想3:气体可能为CO2和SO2的混合气体(2分)
【实验探究】
(1)B(2分)(2)检验SO2气体(2分)(3)检验CO2气体(2分)
【得出结论】SO2和CO2的混合气体(2分)
【提出猜想】
猜想2:气体可能为SO2(2分);猜想3:气体可能为CO2和SO2的混合气体(2分)
【实验探究】
(1)B(2分)(2)检验SO2气体(2分)(3)检验CO2气体(2分)
【得出结论】SO2和CO2的混合气体(2分)
略

练习册系列答案
相关题目
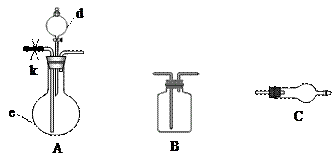
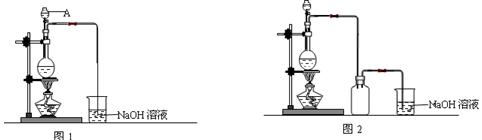
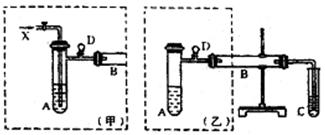

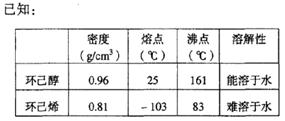
 口进入。蒸馏时要加入生石灰,目的是 。
口进入。蒸馏时要加入生石灰,目的是 。