题目内容
6.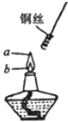 如图,某同学做乙醇氧化实验时,将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰a、b两点时现象明显不同.请你写出a、b两点的实验现象,并解释产生该现象的原因,并写出化学反应方程式.
如图,某同学做乙醇氧化实验时,将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰a、b两点时现象明显不同.请你写出a、b两点的实验现象,并解释产生该现象的原因,并写出化学反应方程式.| 实验现象 | 解释 | 化学方程式 | |
| a | |||
| b |
分析 a处,加热条件下,Cu和空气中氧气反应生成黑色的CuO;
b处含有挥发出的乙醇,加热条件下,乙醇和CuO发生氧化反应生成乙醛和Cu,据此分析解答.
解答 解:a处乙醇充分燃烧导致温度高,加热条件下,Cu和空气中氧气反应生成黑色的CuO,所以看到的现象是铜丝变黑,反应方程式为2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;
b处含有挥发出的乙醇,加热条件下,乙醇和CuO发生氧化反应生成有刺激性气味的乙醛和红色的Cu,
所以实验的现象是:铜丝又变为红色,并有刺激性气味的气体产生,反应方程式为CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O,
故答案为:
| 实验现象 | 解释 | 化学方程式 | |
| a | 铜丝变黑 | 外焰处乙醇充分燃烧,铜丝被氧化 | 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO |
| b | 铜丝又变为红色,并有刺激性气味的气体产生 | 焰心处乙醇未充分燃烧,CuO被还原,乙醇氧化得到乙醛 | CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O |
点评 本题考查乙醇的催化氧化,侧重考查学生分析判断及实验操作能力,明确各个部分发生的反应是解本题关键,知道乙醇的催化氧化中Cu在作用,注意“催化剂实际上参加反应”,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.水体中重金属铅的污染问题备受关注.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形态的浓度分数α随溶液pH变化的关系如图所示:
[1表示Pb2+、2表示Pb(OH)+、3表示Pb(OH)2、4表示Pb(OH)3-、5表示Pb(OH)42-]
(1)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液存在的阳离子除H+、Na+外,还有:Pb2+、Pb(OH)+.
(2)pH=9时主要反应的离子方程式是:Pb(OH)++OH-?Pb(OH)2↓
(3)某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
上表中除 Pb2+外,该脱铅剂对其他离子的去除效果最好的是:Fe3+
(4)如该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:2EH(s)+Pb2+?E2Pb(s)+2H+
则脱铅最合适的pH范围为B(填代码).
A.4~5 B.6~7 C.9~10 D.11~12.
[1表示Pb2+、2表示Pb(OH)+、3表示Pb(OH)2、4表示Pb(OH)3-、5表示Pb(OH)42-]
(1)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液存在的阳离子除H+、Na+外,还有:Pb2+、Pb(OH)+.
(2)pH=9时主要反应的离子方程式是:Pb(OH)++OH-?Pb(OH)2↓
(3)某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
| 离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度(mg/L) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度(mg/L) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
(4)如该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:2EH(s)+Pb2+?E2Pb(s)+2H+
则脱铅最合适的pH范围为B(填代码).
A.4~5 B.6~7 C.9~10 D.11~12.

12.能正确表示下列化学反应的离子方程式是( )
| A. | 单质铁与盐酸的反应 Fe+2 H+=Fe2++H2↑ | |
| B. | 氨水跟硫酸发生酸碱中和反应 OH-+H+=H2O | |
| C. | 铜片插入硝酸银溶液中Cu+Ag+=Cu2++Ag | |
| D. | 碳酸钙加入醋酸溶液中 CaCO3+2CH3COOH=CO2↑+2CH3COO-+H2O+Ca2+ |
14.下表中金属的冶炼原理与方法不完全正确的是( )
| 冶炼原理 | 方法 | |
| A | 2HgO$\frac{\underline{\;加热\;}}{\;}$2Hg+O2↑ | 热分解法 |
| B | 2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑ | 电解法 |
| C | Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2 | 热分解法 |
| D | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | 热还原法 |
| A. | A | B. | B | C. | C | D. | D |
1.下列各组物质中,化学键类型和化合物类型都相同的是( )
| A. | CO2和Na2CO3 | B. | SO2和H2O | C. | KOH和NaCl | D. | NaCl和HCl |
11.下列电离方程式中,正确的是( )
| A. | NH3•H2O?NH+4+OH- | B. | KClO3=K++Cl-+3O2- | ||
| C. | H2CO3=2H++CO32- | D. | Ba(OH)2=Ba2++OH- |
18.下列比较正确的是 ( )
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④碱性:Ca(OH)2>Mg(OH)2.
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④碱性:Ca(OH)2>Mg(OH)2.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
15.下列属于吸热反应的是( )
| A. | Ba(OH)2•8H2O和NH4Cl(s)混合反应 | B. | 生石灰和水的反应 | ||
| C. | 液态水气化 | D. | 盐酸与氢氧化钠溶液的反应 |
16.下列各组物质中,不管它们以何种比例混合,只要总质量一定,充分燃烧后生成的二氧化碳的量不变的是( )
| A. | 乙烷和苯 | B. | 乙醇和丙醇 | C. | 乙醇和乙醚 | D. | 甲醛和乙酸 |