题目内容
11.水体中重金属铅的污染问题备受关注.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形态的浓度分数α随溶液pH变化的关系如图所示:[1表示Pb2+、2表示Pb(OH)+、3表示Pb(OH)2、4表示Pb(OH)3-、5表示Pb(OH)42-]
(1)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液存在的阳离子除H+、Na+外,还有:Pb2+、Pb(OH)+.
(2)pH=9时主要反应的离子方程式是:Pb(OH)++OH-?Pb(OH)2↓
(3)某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
| 离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度(mg/L) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度(mg/L) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
(4)如该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:2EH(s)+Pb2+?E2Pb(s)+2H+
则脱铅最合适的pH范围为B(填代码).
A.4~5 B.6~7 C.9~10 D.11~12.

分析 (1)由图象可知pH=8时,Pb2+,Pb(OH)+和Pb(OH)2共存;
(2)pH=9时,曲线2、3表示的物质共存,由图可知Pb(OH)2的浓度分数比Pb(OH)+的大,所以主要反应是生成Pb(OH)2;
(3)根据浓度变化判断处理效果;
(4)根据反应判断,参加反应的是Pb2+,由图象可知,选择PH要使铅全部以Pb2+形式存在.
解答 解:(1)由图象可知pH=8时,Pb2+,Pb(OH)+和Pb(OH)2共存,另外溶液中还有H+,所以中存在的阳离子(除H+、Na+外)有Pb2+、Pb(OH)+,
故答案为:Pb2+、Pb(OH)+;
(2)pH=9时,曲线2、3表示的物质共存,由图可知Pb(OH)2的浓度分数比Pb(OH)+的大,所以主要反应是生成Pb(OH)2,反应的方程式为Pb2++2OH-═Pb(OH)2↓,
故答案为:Pb(OH)++OH-?Pb(OH)2↓;
(3)加入脱铅剂,Pb2+浓度转化率为$\frac{0.1-0.004}{0.1}$=96%,Fe3+浓度转化率为$\frac{0.12-0.04}{0.12}$=67%,而其它两种离子转化率较小,则除Pb2+外,该脱铅剂对其它离子的去除效果最好的是Fe3+,
故答案为:Fe3+;
(4)反应为2EH(s)+Pb2+?E2Pb(s)+2H+,参加反应的是Pb2+,由图象可知,选择PH要使铅全部以Pb2+形式存在,应为6~7之间,
故答案为:B.
点评 本题以Pb2+在水溶液中的各种形态与溶液中pH变化关系图,考查了学生在对多重平衡的函数曲线理解,是一个典型的利用多元信息,综合性考查学生知识与能力的创新型题目,题目难度中等.

练习册系列答案
相关题目
1.中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示,下列叙述正确的是( )

| A. | M的相对分子质量是180 | |
| B. | M与足量的NaOH溶液发生反应时,所得的有机产物的化学式C9H4O5Na4 | |
| C. | 1molM最多能与2molBr2发生反应 | |
| D. | 1molM与足量NaHCO3反应能生成2molCO2 |
2.下列实验基本操作正确的是( )
| A. | 经实验测定等物质的量的盐酸、醋酸分别与足量NaOH溶液反应放出的热量相等 | |
| B. | 中和热测定实验中可以用环形铁丝搅拌棒代替环形玻璃搅拌棒 | |
| C. | 用碱式滴定管量取0.10 mol•L-1的Na2CO3溶液22.10 mL | |
| D. | 用玻璃棒蘸取溶液滴到湿润的广范pH试纸上,测其pH=3.6 |
19.海水提溴过程中,将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生作用以达到富集的目的,化学反应为Br2+SO2+2H2O═2HBr+H2SO4,下列说法正确的是( )
| A. | Br2在反应中表现氧化性 | B. | SO2在反应中被还原 | ||
| C. | Br2在反应中得电子 | D. | 1mol氧化剂在反应中得到1mol电子 |
6.已知:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ•mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ•mol-1
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是( )
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ•mol-1
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是( )
| A. | 1:1 | B. | 2:3 | C. | 1:4 | D. | 1:3 |
16.4.48L一定条件下的氯化氢气体通入水中得到0.1L盐酸,此溶液中c(Cl-)=2mol/L,则“一定条件”可能是( )
| A. | 25℃ | B. | 1.01×103Pa | C. | 101kPa | D. | 0℃ |
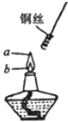 如图,某同学做乙醇氧化实验时,将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰a、b两点时现象明显不同.请你写出a、b两点的实验现象,并解释产生该现象的原因,并写出化学反应方程式.
如图,某同学做乙醇氧化实验时,将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰a、b两点时现象明显不同.请你写出a、b两点的实验现象,并解释产生该现象的原因,并写出化学反应方程式.