题目内容
【题目】H2O2(l)在有MnO2条件下和无MnO2条件下分解的能量变化如图所示。下列说法正确的是
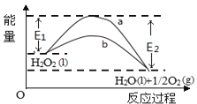
A. 有MnO2 条件下的反应曲线是a曲线
B. 该反应能量变化类型与CaCO3分解反应相同
C. 加催化剂后,正反应速率加快,逆反应速率减小
D. b曲线的热化学方程式为:H2O2(l) =H2O(l) +1/2O2(g) ΔH= ( E1 - E2 )kJmol-1
【答案】D
【解析】
A. 催化剂降低反应活化能而改变反应速率,但不影响平衡移动,则焓变不变,所以有MnO2条件下的反应曲线是b曲线,故A错误;B. 该反应反应物能量高,生成物能量低,为放热反应,CaCO3分解是吸热反应,故B错误;C.加催化剂后正逆反应速率同时增大,故C错误;D. 该反应的焓变为△H=(E1E2)KJmol1或△H=(E2E1)KJmol1,故D正确;本题选D。

练习册系列答案
相关题目