��Ŀ����
����Ŀ�������Ǹ�ˮ����[Cr(CH3COO)2]2��2H2O��һ���������ռ���Ϊ����ɫ���壬�ױ������������Ҵ���������ˮ������(�ӷ����л��ܼ�)�����Ʊ�װ�ü��������£�
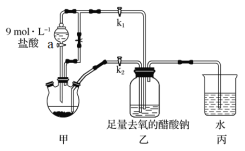
�ټ��װ�������Ժ���������ƿ�����μ������п��������CrCl3��Һ��
�ڹر�k2��k1������a�����������ƺõ��١�
�۴�������ƿ�ڵ���Һ������ɫ(Cr3��)��Ϊ����ɫ(Cr2��)ʱ������Һת�Ƶ�װ�����У������ִ�������ɫ����ʱ���ر�a��������
�ܽ�װ�����л������ٹ��ˡ�ϴ�Ӻ��������
��1��ʵ������������ˮ�辭��к�Ѹ����ȴ��Ŀ����________________________������a��������__________��
��2��������ƿ�е�Zn��������������H2�⣬��������һ����Ӧ�����ӷ���ʽΪ____________��
��3��ʵ�鲽�������Һ�Զ�ת����װ�����е�ʵ�����Ϊ___________________��
��4��װ�ñ��е��ܿ�ˮ���Ŀ����______________________________________��
��5��Ϊϴ��[Cr(CH3COO)2]2��2H2O��Ʒ�����з���������ʵ���________��
a����������ϴ������ˮϴ b������ˮϴ����������ϴ
c������ˮϴ�������Ҵ�ϴ d�������Ҵ�ϴ����������ϴ
��6��һ�������£�[Cr(CH3COO)2]2��2H2O���ȵõ�CO��CO2�Ļ�����壬�����ʵ�����CO�Ĵ���_____________________________________________��
���𰸡���ȥˮ�е��ܽ��� ��Һ©�� Zn��2Cr3��===2Cr2����Zn2�� �ر�k1����k2 ��ֹ��������װ����������Cr2�� b �������ͨ�����ȵ�CuO��������ɫ�ɺ�ɫ��Ϊ��ɫ��˵����������к���CO(���������𰸾���)
��������
װ�üף���Һ©��ʢװϡ���ᣬ��Բ����ƿ��п�����ᷴӦZn+2HCl�TZnCl2+H2����ͬʱ����2CrCl3+Zn�T2CrCl2+ZnCl2��������������������ѹǿ�����ɵ�CrCl2��Һѹ��װ�����У�װ���ң�2Cr2++4CH3COO-+2H2O�T[Cr��CH3COO��2]22H2O��װ�ñ��DZ���װ��ѹǿƽ�⣬ͬʱ����������룻��1������[Cr(CH3COO)2]2��2H2O�ױ�������������ˮ�辭��к�Ѹ����ȴ��Ŀ��������װ��ͼ��������a�����ƣ���2������������ƿ�з����ķ�Ӧ���з�������3��ʵ�鿪ʼ����H2����Ϊʹ���ɵ�CrCl2��Һ��CH3COONa��Һ˳����ϣ���K2�ر�K1�������ɵ�CrCl2��Һѹ��װ��3�У���4������[Cr(CH3COO)2]2��2H2O�ױ���������װ�ñ��е��ܿ�ˮ���Ŀ������5�������Ǹ�ˮ���ﲻ������ˮ���ѣ����ڴ������������ᣬ�ݴ�ѡ��ϴ���Լ�����7��CO�ܻ�ԭ���ȵ�����ͭ���ݴ���Ƽ���CO�ķ�����
��1�� [Cr(CH3COO)2]2��2H2O�ױ���������������ˮ�辭��к�Ѹ����ȴ��Ŀ���dz�ȥˮ�е��ܽ���������װ��ͼ������a�������Ƿ�Һ©������2��������ƿ�е�Zn��������������H2�⣬ͬʱ����2CrCl3+Zn�T2CrCl2+ZnCl2�����ӷ���ʽΪ2Cr3++Zn�T2Cr2++Zn2+����3��ʵ�鿪ʼ����H2����Ϊʹ���ɵ�CrCl2��Һ��CH3COONa��Һ˳����ϣ���K2�ر�K1�������ɵ�CrCl2��Һѹ��װ�����з�Ӧ����4�� [Cr(CH3COO)2]2��2H2O�ױ�������װ�ñ��е��ܿ�ˮ���Ŀ���Ƿ�ֹ��������װ����������Cr2������5�������Ǹ�ˮ���ﲻ������ˮ���ѣ����ڴ������������ᣬ��������ˮϴ����������ϴ��ѡb����7���������ͨ�����ȵ�CuO��������ɫ�ɺ�ɫ��Ϊ��ɫ��˵����������к���CO��

 ����ʦ���һ��һ��ϵ�д�
����ʦ���һ��һ��ϵ�д�