题目内容
【题目】肼(N2H4)是一种无色易溶于水的油状液体,具有碱性和极强的还原性,在工业生产中应用非常广泛。

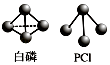
(1)已知肼的球棍模型如图所示,写出肼的电子式:____________。
(2)已知1g肼(N2H4)气体燃烧生成氮气和水蒸气,放出16.7kJ的热量。写出该反应的热化学方程式:______________。
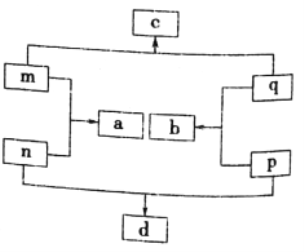
(3)目前正在研发的一-种肼燃料电池的结构如下图所示。

①该电池的负极是______(填“a”或“b”)电极。
②写出正极的电极反应式:_____________。
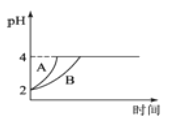
(4)在1L固定体积的容器中加入0.1molN2H4,在303K、Pt催化下发生反应:N2H4(l) ![]() N2(g)+2H2(g)。测得容器中
N2(g)+2H2(g)。测得容器中![]() 与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=______。
与时间关系如下图所示,则0~4min内氮气的平均反应速率v(N2)=______。

【答案】 ![]() N2H4(g)+O2(g)=N2(g)+2H2O(g) H=-534.4kJ/mol a O2+4e-+2H2O=4OH- 0.0125mol/(L·min)
N2H4(g)+O2(g)=N2(g)+2H2O(g) H=-534.4kJ/mol a O2+4e-+2H2O=4OH- 0.0125mol/(L·min)
【解析】(1)氨分子中氢原子被氨基(-NH2)取代后的生成物叫肼,分子中全部为单键;(2)正极是氧气得电子发生还原反应,负极肼失电子发生氧化反应;(3)在303K , Pt催化下,则发生N2H4(l) ![]() N2(g)+2H2(g),设生成氮气的量为xmol,则氢气的量为2mol,此时N2H4(l)的物质的量为(0.1-x)mol ,根据4min 时比值为3,求出x的值,然后根
N2(g)+2H2(g),设生成氮气的量为xmol,则氢气的量为2mol,此时N2H4(l)的物质的量为(0.1-x)mol ,根据4min 时比值为3,求出x的值,然后根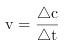 计算。
计算。
(1)由肼的球棍模型和价键理论可知,肼中氮氮原子之间、氮氢原子之间都是单键,所以肼的电子式为: ![]() 。答案:
。答案:![]() 。
。
(2)已知1g肼(N2H4)气体燃烧生成氮气和水蒸气,放出16.7kJ的热量。则1mol肼(N2H4)气体燃烧生成氮气和水蒸气,放出534.4kJ 的热量,所以肼反应的热化学方程式: N2H4(g)+O2(g)=N2(g)+2H2O(g) H=-534.4kJ/mol 。
(2)正极是氧气得电子发生还原反应,负极肼失电子发生氧化反应,所以a电极为电池的负极,因此,答案是:a。
(3)在303K、Pt催化下,则发生N2H4(l) ![]() N2(g)+2H2(g),设生成氮气的量为xmol,则氢气的量为2mol,此时N2H4(l)的物质的量为(0.1-x)mol,根据4min时比值为3,所以3x/(0.1-x)=3,则x=0.05mol,
N2(g)+2H2(g),设生成氮气的量为xmol,则氢气的量为2mol,此时N2H4(l)的物质的量为(0.1-x)mol,根据4min时比值为3,所以3x/(0.1-x)=3,则x=0.05mol,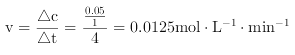 ,因此,本题正确答案是: 0.0125mol/(L·min)。
,因此,本题正确答案是: 0.0125mol/(L·min)。