题目内容
【题目】设 NA 为阿伏加德罗常数的值。下列说法正确的是
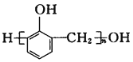
A.0.l mol C2H6O 分子中含 C-H 键数目为 0.5 NA
B.1 mol·L-1 的 NH4Cl 溶液中含有![]() 数目小于 0.1 NA
数目小于 0.1 NA
C.25℃时,1 L pH=13 的 Ba(OH)2 溶液中含有 OH-的数目为 0.2NA
D.1 mol Cl2 与足量铜铁合金反应,转移电子数一定是 2 NA
【答案】D
【解析】
A.0.lmolC2H6O分子中含C-H键数目不一定为0.5NA,若该分子式表示为乙醇,一个乙醇分子中含C-H键数目为5个,则0.1mol中含有C-H键数目为0.5NA;若该分子是表示的是二甲醚,一个二甲醚分子中含有6个C-H,则0.1mol含有C-H键数目为0.6NA,A选项错误;
B.题中为给出该溶液的体积,溶质的物质的量无法求解,![]() 的数目无法判断,B选项错误;
的数目无法判断,B选项错误;
C.pH=13的Ba(OH)2溶液,OH-的浓度为0.1mol·L-1,体积为1L,则OH-的物质的量=0.1mol·L-1×1L=0.1mol,其数目为0.1NA,C选项错误;
D.1molCl2与足量铜铁合金反应,氯气完全反应,Cl元素由0价变为-1价,一个氯气分子转移2个电子,则1mol Cl2完全反应转移电子数为2NA,D选项正确;
答案选D。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】实验室用硼镁泥为原料制取MgSO4·7H2O粗产品的过程如下:
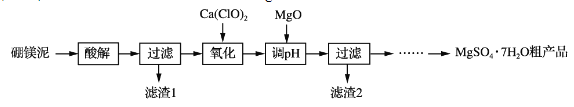
硼镁泥的主要成分如下表:
MgO | SiO2 | FeO、Fe2O3 | CaO | Al2O3 | B2O3 |
30%~40% | 20%~25% | 5%~15% | 2%~3% | 1%~2% | 1%~2% |
(1)“酸解”时为提高Mg2+的浸出率,可采用的措施是_____(写一种)。所加酸不宜过量太多的原因是_____。
(2)“氧化”步骤中,若用H2O2代替Ca(ClO)2,则发生反应的离子方程式为______________。实际未使用H2O2,除H2O2成本高外,还可能的原因是______________________________________。
(3)“调pH”时用MgO而不用NaOH溶液的原因是________________________。
(4)结合附表信息,由MgSO4·7H2O粗产品(含少量CaSO4)提纯获取MgSO4·7H2O的实验方案如下:将粗产品溶于水,_________________________________________________,室温下自然挥发干燥。(实验中必须使用的试剂有:饱和MgSO4溶液,乙醇)附:两种盐的溶解度(g/100 g水)
温度℃ | 10 | 30 | 40 | 50 |
CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 |
MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 |
【题目】利用下图装置做下面的实验:在烧杯中盛有半杯乙溶液,然后用滴定管向容器中滴入甲溶液。随着甲的滴入,灯泡逐渐变暗;滴到一定量时,灯泡熄灭,继续滴入甲溶液,灯泡又逐渐变亮。下列各组溶液中,能够产生上述现象的是 ( )
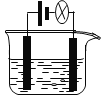
选项 | 甲 | 乙 |
A | NH3·H2O | HCl |
B | CH3COOH | NH3·H2O |
C | NaOH | MgCl2 |
D | H2SO4 | Ba(OH)2 |
A.AB.BC.CD.D