题目内容
4.如图为元素周期表中短周期的一部分,若X原子次外层电子数比最外层电子数多3,则下列说法正确的是( )| R | ||
| X | Y | Z |
| A. | X的氢化物比R的氢化物稳定 | |
| B. | 原子半径大小顺序是Z>Y>X | |
| C. | Y元素能形成两种常见的含氧酸,其中一种是强酸 | |
| D. | XZ5分子中各原子均满足最外层8电子结构 |
分析 图为元素周期表中短周期的一部分,可知R处于第二周期,X、Y、Z处于第三周期,X原子次外层电子数比最外层电子数多3,则X为P元素,可推知R为O元素、Y为S元素、Z为Cl.
A.非金属性越强,氢化物越稳定;
B.同周期自左而右原子半径减小;
C.硫元素形成的常见两种含氧酸为亚硫酸、硫酸,其中硫酸为强酸;
D.若元素原子最外层电子数+化合价绝对值=8,该原子满足8电子结构.
解答 解:图为元素周期表中短周期的一部分,可知R处于第二周期,X、Y、Z处于第三周期,X原子次外层电子数比最外层电子数多3,则X为P元素,可推知R为O元素、Y为S元素、Z为Cl.
A.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故X的非金属性比R的弱,非金属性越强,氢化物越稳定,故X的氢化物不如R的氢化物稳定,故A错误;
B.同周期自左而右原子半径减小,故原子半径:X>Y>Z,故B错误;
C.硫元素形成的常见两种含氧酸为亚硫酸、硫酸,其中硫酸为强酸,故C正确;
D.PCl5分子中P原子最外层电子数为5,化合价为+5,二者之和为10,分子中P原子最外层电子数为10,不满足8电子结构,故D错误,
故选C.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素周期律的理解应用.

练习册系列答案
相关题目
19.下列有机物命名正确的是( )
| A. |  2-甲基-2-氯丙烷 | B. |  1,3,4-三甲苯 | C. | 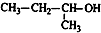 2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 |
13.在体积可变的密闭容器中,反应mA(g)+nB(s)?qC(g)达到平衡后,压缩容器体积,发现A的转化率降低,下列说法中,正确的是( )
| A. | (m+n)必定小于q | B. | (m+n)必定大于q | C. | m必定小于q | D. | m必定大于q |
14.烷烃 是由某单烃与H2加成后的产物,(考虑时包括烯烃的顺反异构),则这种但烯烃的结构可能有( )
是由某单烃与H2加成后的产物,(考虑时包括烯烃的顺反异构),则这种但烯烃的结构可能有( )
 是由某单烃与H2加成后的产物,(考虑时包括烯烃的顺反异构),则这种但烯烃的结构可能有( )
是由某单烃与H2加成后的产物,(考虑时包括烯烃的顺反异构),则这种但烯烃的结构可能有( )| A. | 4种 | B. | 5种 | C. | 7种 | D. | 9种 |
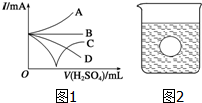
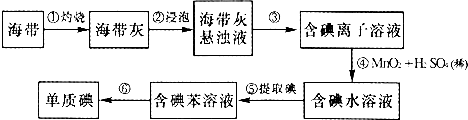

 中和热是指酸跟碱发生中和反应生成l mol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
中和热是指酸跟碱发生中和反应生成l mol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题: