题目内容
3.下列说法正确的是( )| A. | 金属腐蚀就是金属原子失去电子被还原的过程 | |
| B. | 镀锌铁皮的镀层损坏后,铁还是受到保护而难以腐蚀 | |
| C. | 钢铁的腐蚀通常有吸氧腐蚀和析氢腐蚀,通常情况下以吸氧腐蚀为主 | |
| D. | 氯碱工业中,阳极发生的反应为:2H++2e-═H2↑ |
分析 A、金属原子失去电子,化合价升高,在反应中被氧化;
B、形成原电池后的装置中,负极金属易被腐蚀,正极金属被保护;
C、钢铁是碳和铁的合金易发生电化学腐蚀;
D、氯碱工业中,阳极发生的反应为:2Cl--2e-═Cl2↑
解答 解:A、金属腐蚀就是金属原子失去电子被氧化的过程,故A错误;
B、镀锌铁皮的镀层损坏后,会形成原电池,金属铁是正极,被保护,不容易腐蚀,故B错误;
C、钢铁是碳和铁的合金易发生电化学腐蚀,酸性条件下发生析氢腐蚀,弱酸性、中性条件下发生吸氧腐蚀,通常情况下以吸氧腐蚀为主,故C正确;
D、氯碱工业中,阳极发生的反应为:2Cl--2e-═Cl2↑,故D错误;
故选C.
点评 本题考查学生金属的腐蚀和防护知识,注意原电池原理的应用以及金属腐蚀的实质,属于教材知识的考查,难度不大.

练习册系列答案
相关题目
13.下列物质中,既含有极性共价键又含有非极性共价键的是( )
| A. | CH4 | B. | C2H4 | C. | NaCl | D. | HCl |
11.2005年6月,国内某知名媒体报道,国内啤酒生产企业中95%以上在生产过程中都填加了甲醛作为添加剂,在啤酒行业内引起极大反响.下列关于甲醛的说法中正确的是( )
| A. | 甲醛分子组成中仅有C、H两种元素 | |
| B. | 甲醛是一种无色无味的气体,对人体无危害,所以,可以放心饮用啤酒 | |
| C. | 甲醛的化学性质很稳定,很难与强酸、强碱、强氧化剂反应 | |
| D. | 甲醛既可以被氧化生成甲酸、也可以还原生成甲醇 |
18.已知热化学方程式:C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(g)△H=-1256kJ•mol-1.下列说法正确的是( )
| A. | C2H2的燃烧热为1256kJ/mol | |
| B. | 若生成2mol液态水,则△H=-2512kJ/mol | |
| C. | 若转移10mol电子,则消耗2.5mol O2 | |
| D. | 若形成4mol碳氧共用电子对,则放出的热量为2512kJ |
8.用铂(惰性)电极进行电解,下列说法中正确的是( )
| A. | 电解稀硫酸溶液,实质上是电解水,故溶液pH不变 | |
| B. | 电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 | |
| C. | 电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1:2 | |
| D. | 电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 |
12.关于下列各图的叙述中,正确的是( )
| A. | 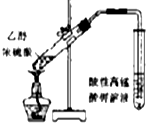 如图装置检验加热时产生的乙烯 | |
| B. | 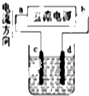 如图装置精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液. | |
| C. | 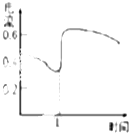 如图表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2 | |
| D. | 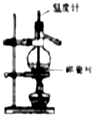 如图装置分离溴的四氯化碳溶液 |
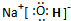 物质I是极性分子(填极性或非极性)
物质I是极性分子(填极性或非极性)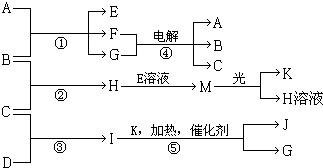
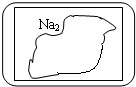 现有一盛有无色固体物质M的试剂瓶,标签已破损(见图).
现有一盛有无色固体物质M的试剂瓶,标签已破损(见图).
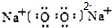 ; D的结构式O=C=O.
; D的结构式O=C=O.