题目内容
【题目】氢气作为新能源,广泛应用于能源、化学等领域。现阶段氢气主要通过天然气重整的方式进行工业生产。发生的化学方程式如下:
反应I CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206 kJ/mol
CO(g)+3H2(g) △H1=+206 kJ/mol
反应II CO(g)+H2O(g)![]() CO2(g)+H2(g) △H2=-41 kJ/mol
CO2(g)+H2(g) △H2=-41 kJ/mol
副反应 CH4(g)![]() C(s)+2H2(g) △H3=+75 kJ/mol
C(s)+2H2(g) △H3=+75 kJ/mol
(1)①若仅发生反应I,为提高CH4的平衡转化率,宜采用的反应条件为_________。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
②某研究小组在一定条件下往恒温恒容的密闭容器中通入一定量的甲烷和水蒸气,实验过程中发现CO2的产率远大于CO的产率,请解释可能的原因________________。
(2)在实际生产过程中,科学家发现使用Ni作为催化剂(当Ni表面吸附大量碳时,会导致催化剂活性下降),可加快反应I的反应速率,从而加快整个反应的进行,提高单位时间内H2的产率。
①某恒容体系中,压强为1.3MPa,水/甲烷的物质的量之比为4,反应相同时间,H2的物质的量随反应温度的变化曲线如图所示。
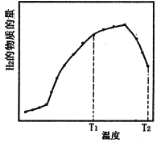
下列说法正确的是__________
A.对反应I而言,KT1>KT2
B.水/甲烷的物质的量之比等于4,大于初始反应的化学计量数之比,有利于促进CH4的转化,同时也有利于CO转化为CO2
C.使用Ni做催化剂,可增加活化分子百分数,从而加快反应速率,其主要原因是提高分子自身所具有的能量
D.若控制其他条件不变,缩小体积,则CH4的平衡转化率将减小
②在某恒温体系中,体积为1L,水/甲烷的物质的量之比等于4,投入CH4的量为l mol,若仅发生上述一系列反应,一段时间后,测得CH4的转化率为a,其中生成CO的选择性(转化的CH4中,生成CO的百分含量)为b,CO2的浓度为c mol/L,求此时H2的物质的量浓度为___________,CO的物质的量浓度为______________
(3)现科学家发现,以Ni-CaO为复合催化剂能在一定程度上促进天然气重整反应的正向进行,使H2体积分数达到95%左右。请从能量利用及平衡移动角度,理论分析以Ni-CaO为复合催化剂的优点_____________________________________________。
(4)CH4自身也可做为然料电池的原料,其工作原理如图所示。
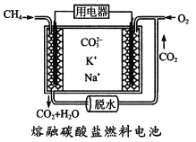
请写出通入甲烷-极的电极反应式为_______________________________________。
【答案】C 反应I的活化能较高,反应II的活化能较低,因此生成的CO被迅速转化为二氧化碳不能积累 BD (ab+c+2a)mol/L (ab-c)mol/L 氧化钙可吸附二氧化碳,使I的平衡正向移动,提高氢气的产率;同时,氧化钙吸附二氧化碳是放热反应,可为反应I的进行提供热量,降低系统能耗。 ![]()
【解析】
(1)①由于反应I为吸热反应,且为气体体积增大的反应,故为了提高CH4的平衡转化率,宜采用的反应条件为高温低压,答案选C;
②在一定条件下往恒温恒容的密闭容器中通入一定量的甲烷和水蒸气, CO2的产率远大于CO的产率,是由于反应I的活化能较高,反应II的活化能较低,因此生成的CO被迅速转化为二氧化碳不能积累;
(2)①A. 反应I为吸热反应,故对反应I而言,KT1<KT2,A错误;
B. 水/甲烷的物质的量之比等于4,大于初始反应的化学计量数之比,有利于促进CH4的转化,同时也有利于CO转化为CO2,B正确;
C. 使用Ni做催化剂,可增加活化分子百分数,从而加快反应速率,其主要原因是降低了反应的活化能,C错误;
D. 由于反应I为气体体积增大的反应,若控制其他条件不变,缩小体积,则CH4的平衡转化率将减小,D正确;
故答案选BD;
②生成CO的选择性(转化的CH4中,生成CO的百分含量)为b,则反应I消耗的甲烷的物质的量浓度为ab mol/L,生成的氢气为3ab mol/L,由于CO2的浓度为c mol/L,则反应II生成氢气的浓度为c mol/L,反应III甲烷的消耗量为a(1-b),则生成的氢气的浓度为2a(1-b),则生成氢气的总浓度为(ab+c+2a)mol/L,反应I生成的CO的浓度为ab,反应II消耗的CO的浓度为c,则生成的CO浓度为(ab-c)mol/L;
(3)以Ni-CaO为复合催化剂的优点为氧化钙可吸附二氧化碳,使I的平衡正向移动,提高氢气的产率;同时,氧化钙吸附二氧化碳是放热反应,可为反应I的进行提供热量,降低系统能耗;
(4)甲烷在该燃料电池中作负极,电极反应为![]() 。
。