题目内容
【题目】下列实验方案设计及结论均正确的是( )
A.淀粉溶液![]() 水解液
水解液![]() 为蓝。结论:淀粉完全没有水解
为蓝。结论:淀粉完全没有水解
B.淀粉溶液![]() 水解液
水解液![]() 无砖红色沉淀。结论:淀粉完全水解
无砖红色沉淀。结论:淀粉完全水解
C.淀粉溶液![]() 水解液
水解液![]() 中和液
中和液![]() 有砖红色沉淀。结论:淀粉已水解
有砖红色沉淀。结论:淀粉已水解
D.淀粉溶液![]() 水解液
水解液![]() 无现象。结论:淀粉没有水解
无现象。结论:淀粉没有水解
【答案】C
【解析】
本题运用到的化学原理是淀粉遇I2变蓝色和淀粉在稀H2SO4催化下水解生成葡萄糖.检验淀粉未水解的关键是实验证明没有水解产物葡萄糖生成;检验淀粉部分水解的关键是既要用实验证明有水解产物葡萄糖生成,还要用实验证明仍有未水解的淀粉存在;检验淀粉水解完全的关键是要用实验证明淀粉已不存在.为使淀粉水解而在淀粉溶液中加入了硫酸,而证明水解产物葡萄糖时,无论用新制Cu(OH)2悬浊液还是银氨溶液都必须在碱性环境中进行,所以在加鉴别试剂前必须用NaOH溶液中和硫酸。
A、加碘水变蓝,说明淀粉未完全水解,不能说明淀粉完全没有水解,结论错误,故A错误;
B、水解液没有加碱中和,所以无法检验葡萄糖的存在,实验设计及结论都错误,故B错误;
C、淀粉在酸性溶液中水解,产物是葡萄糖,中和水解液后用新制氢氧化铜悬浊液检验葡萄糖,有砖红色沉淀,说明淀粉已经水解,实验方案设计及结论都正确,故C正确;
D、水解液没有加碱中和,所以无法检验葡萄糖的存在,实验设计及结论都错误,故D错误。
答案选C。

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案【题目】氮元素的单质和常见的化合物在工、农业生产中用途广泛。
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
N2 | O2 | Ar | CO2 |
-196℃ | -183℃ | -186℃ | -78℃ |
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是______.
(2)雷雨时空气中的N2转化为NO,生成物NO是______色的气体,______(填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应,写出NO2与水反应的化学方程式为__________________.
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气;
①制取氨气的化学方程式为__________________;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为______g;
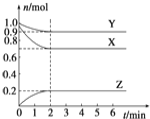
(4)已知:4NH3+6NO![]() 5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能;
5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能; ![]()
若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同);
①NH3与稀硫酸溶液反应的离子方程式为__________________;
②为了比较不同催化剂的催化性能,需要测量并记录的数据是____________。