题目内容
【题目】向等物质的量浓度的HCl、![]() 、
、![]() 、
、![]() 混合溶液中逐滴加入
混合溶液中逐滴加入![]() 的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。下列有关说法正确的是
的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。下列有关说法正确的是 ![]()
![]()

A.在![]() 段加入的NaOH溶液与
段加入的NaOH溶液与![]() 反应
反应
B.在![]() 段加入NaOH溶液发生反应的离子方程式为
段加入NaOH溶液发生反应的离子方程式为![]()
C.在![]() 段加入NaOH溶液发生反应的离子方程式为
段加入NaOH溶液发生反应的离子方程式为![]()
D.在滴加NaOH溶液全过程中主要粒子参与反应的先后顺序是![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]()
【答案】D
【解析】
氢氧化钠首先中和盐酸,然后沉淀金属阳离子,再与氯化铵反应,最后溶解氢氧化铝;
A.在![]() 段加入的NaOH溶液只与盐酸反应,故A错误;
段加入的NaOH溶液只与盐酸反应,故A错误;
B.根据上述分析,在![]() 段加入NaOH溶液发生反应的离子方程式为
段加入NaOH溶液发生反应的离子方程式为 ![]() 和
和![]() ,故B错误;
,故B错误;
C.在![]() 段加入NaOH溶液发生的反应为氢氧化铝的溶解,离子方程式为
段加入NaOH溶液发生的反应为氢氧化铝的溶解,离子方程式为![]() ,故C错误;
,故C错误;
D.在滴加NaOH溶液全过程中主要粒子参与反应的先后顺序是![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,故D正确;
,故D正确;
答案选D。

 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
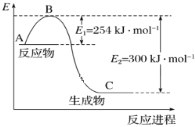
(1)上图是![]() 和
和![]() 反应生成
反应生成![]() 过程中能量的变化示意图,下列有关说法正确的是_______。
过程中能量的变化示意图,下列有关说法正确的是_______。
a. 反应物的总能量比生成物的总能量高
b. 反应物的活化能比生成物的活化能高
c. 反应物的总键能比生成物的总键能高
d. 该反应为熵增反应
(2)请写出![]() 和
和![]() 反应的热化学方程式:_______,决定该反应进行方向的主要判据为________。
反应的热化学方程式:_______,决定该反应进行方向的主要判据为________。
(3)试根据表中及图中数据计算![]() 的键能______________ kJ/mol;
的键能______________ kJ/mol;
化学键 |
|
|
键能/ kJ/mol | 390 | 943 |
(4)用![]() 催化还原
催化还原![]() 还可以消除氮氧化物的污染。已知:
还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=-akJ/mol
N2(g)+O2(g)=2NO(g);△H2=-bkJ/mol
若1molNH3还原NO至N2,则该反应过程中的反应热△H3=_____________kJ/mol(用含a、b的式子表示)。
【题目】温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)===PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A. 反应在前50 s的平均速率v(PCl3)=0.0032 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的ΔH<0
C. 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%